abcsite.free.fr
![]()
Chimie Organique
|
|
3. Alcanes
| Dans ce chapitre | |
| 3.1. | Les chaînes carbonées |
| 3.2. | La nomenclature UICPA, normes 1992 et 1996 (Favre) |
| 3.3. | Propriétés physiques des alcanes |
| 3.4. | Analyse conformationnelle |
| 3.5. | Réactivité des alcanes |
| 3.6. | Hydrocarbures cycliques |
| 3.7. | Erratum du livre "Les Fondements de la Nomenclatue de la Chimie Organique" |
| 3.8. | Exercices de nomenclature |
| Modèles Moléculaires en format .pdb: Alcanes | |
| Modèles Moléculaires en format .pdb: Cycloalcanes | |
3.1. Les chaînes carbonées (Vollhardt 2.2)
Les alcanes sont des hydrocarbures saturés (pas de liaisons multiples) qui constituent la charpente des molécules plus complexes.
Ils sont représentés par la formule RH, ou R est un groupe alkyle.
Les chaînes hydrocarbonées forment le squelette des innombrables autre composés organiques.
Les alcanes sont classés en divers types daprès leur structure:
les alcanes non branchés, i.e. présentant une chaîne linéaire de formule générale CnH2n+2.
les alcanes branchés ou ramifiés aussi de formule générale CnH2n+2.
les alcanes cycliques, ou cycloalcanes possédant une formule générale CnH2n.
les alcanes complexes possédant plusieurs cycles
La série de molécules qui répond à ces formules générales porte le nom de série homologue (homos en grec signifie même que).
Avec un seul C, i.e. lorsque n=1, il ny a quune seule molécule possible, le méthane:
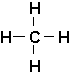
Avec deux (2) C, il ny a encore quune seule forme possible, léthane, car les atomes de carbone ne peuvent être reliés entre eux à laide des atomes dhydrogène qui ne peuvent avoir quune seule liaison:
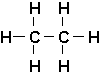
Il en est de même avec trois (3) C, le propane:
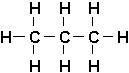
Si lon compare ces trois formules, il appert que lon passe de lune à lautre (dun terme de la série au suivant), en remplaçant un H par un groupe méthyle:
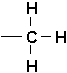
Il faut se rappeler ici que les deux représentations suivantes sont équivalentes:

car lenchaînement est le même: un C portant 2 H entre deux C portant chacun 3 H. Il nexiste donc quune seule formule développée pour les molécules CH4, C2H6, et C3H8.
Lorsque les molécules se compliquent, elles deviennent plus encombrantes et difficile à lire. On utilise donc le plus souvent des formules semi développées:
| Méthane | CH4 |
| Éthane | H3CCH3 |
| Propane | H3CCH2CH3 |
Pour continuer la série et remplacer un H par un CH3, il existe maintenant deux (2) possibilités distinctes et non équivalentes qui diffèrent par le mode denchaînement des atomes et non seulement la façon plane de les écrire:
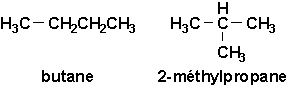
On appelle deux composés comme le butane et le 2-méthylpropane qui possèdent la même formule brute, C4H10, et qui diffèrent par larrangement spatial des atomes des isomères.
Si nous passons aux termes suivants de la série, on trouve trois formules réellement différentes pour les pentanes:
![]()
![]()
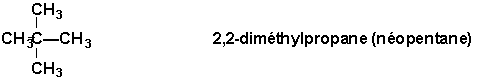
Le nombre disomères possibles pour les alcanes lorsque lon monte dans la série des homologues est indiqué au tableau 2.2 de la page 46 (Vollhardt). Comme on peut le constater, le nombre devient rapidement astronomique.
Il est aussi important de noter que lon peut distinguer les atomes de carbone de types primaire, secondaire, tertiaire et quaternaire selon le nombre datomes de carbones voisins selon:
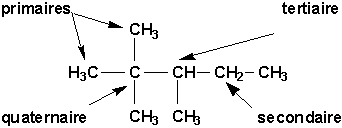
Pour bien différencier toutes ces molécules, il est donc bien important de bien posséder les règles de nomenclature.
3.2. La nomenclature UICPA, normes 1992 et 1996 (Favre)
Nous débuterons cette section par une revue de la nouvelle nomenclature en chimie organique telle quelle a été acceptée par lOrdre des Chimistes du Québec en automne 1992 et modifié à l'été 1996.
Tiré de: Favre, H., "La nomenclature pour la chimie organique. Les noms substitutifs et les noms de classes fonctionnelles, état de la question", 1992.
Tiré de: Favre, H., "Les fondements de la nomenclature pour la chimie organique", 1996
3.2.1. Changements apportés à la nomenclature pour la chimie organique
En 1989, un changement important a été apporté dans la présentation des noms substitutifs et de tout nom faisant appel à ce type de nomenclature. Les indices de position prennent place, maintenant, devant la partie du nom quils qualifient:
propan-2-ol
et non plus propanol-2.De plus, les noms forment maintenant un tout; ils sécrivent dune manière continue, du début à la fin, et non plus, comme auparavant, en blocs séparée:
2-méthylhexane
et non plus méthyl-2 hexane1-iodo-3-méthylhexane
et non plus iodo-1 méthyl-3 hexane.Les symboles R, S, E, Z, cis, trans, etc. se placent également devant ce quils qualifient, que ce soit un nom entier ou une partie seulement dun nom:
cis
-but-2-ène et non plus butène-2-cis(R)-pentan-2-ol
et non plus pentanol-2-(R)3.2.2. Principes, règles et critères en nomenclature substitutive
Une molécule organique est constituée dun
squelette et de groupes fonctionnels. Transposés en termes de
nomenclature substitutive, le squelette devient un hydrure
parental et les groupes fonctionnels des groupes caractéristiques.
Un hydrure parental est à la base de tous les noms substitutifs; les
groupes caractéristiques sont cités par des préfixes
ou des suffixes, selon le schéma qui suit:
|
préfixes |
hydrure parental |
suffixes |
Un examen plus approfondi des préfixes et des suffixes montre quil y a en fait deux types de préfixes et deux types de suffixes. Les préfixes se divisent en préfixes séparables et en préfixes non séparables.
Les préfixes séparables correspondent aux groupes caractéristiques. Ils sont cités les premiers dans un nom et toujours dans lordre alphabétique: chlorométhane.
Les préfixes non séparables jouent un rôle spécifique, en ce quils modifient dune manière permanente les hydrures parentaux de base. Ainsi, dans le nom "cyclohexane", le préfixe cyclo est associé une fois pour toute à lhydrure parental de base hexane, pour nommer une nouvelle entité cyclique qui est un hydrure parental en soi. On aura ainsi "chlorocyclohexane", "méthylcyclohexane".
Les suffixes se divisent en suffixes exclusifs et en suffixes cumulatifs.
Les suffixes exclusifs correspondent aux groupes caractéristiques. Ils sont exclusifs en ce quun seul suffixe est utilisé, à lexclusion de tous les autres. Le choix dun suffixe se fait selon une liste de priorité. Ainsi, un acide carboxylique a priorité sur un alcool, une cétone sur une amine. Lorsque plusieurs groupes caractéristiques représentant des fonctions diverses sont présents, un seul est cité en tant que suffixes, les autres devenant des préfixes.
Les suffixes cumulatifs correspondent aux radicaux, cations, anions, zwittérions. Une entité chimique, à la fois radicalaire et anionique, sera nommé en utilisant les suffixes appropriés à la partie radicalaire et à la partie anionique et en les citant ensemble, selon un ordre donné, à la fin du nom complet.
Le schéma devient ainsi:
|
préfixes séparables |
préfixes non-séparables |
hydrure parental |
suffixes exclusifs |
suffixes cumulatifs |
Un autre aspect doit retenir notre attention. Cest celui de la variation du degré de saturation-insaturation dun composé organique, et la façon de traduire cette variation dans un nom. La variation du degré de saturation-insaturation se fait, en termes de nomenclature, en modifiant le nom de lhydrure parental.
Les hydrures parentaux se divisent en deux catégories: ceux qui sont saturés et ceux qui sont insaturés. Si le degré de saturation est facile à déterminer (il correspond au maximum datomes dhydrogène compatible avec la valence des atomes intéressés) le degré dinsaturation, qui peut être fort variable, est défini, par convention, comme celui qui correspond au maximum de doubles liaisons non cumulées. On exprime cette réalité par lacronyme MADONC (MAximum de DOubles liaisons Non Cumulées). Le benzène et le naphtalène sont des composés de type MADONC et sont utilisés comme tels comme hydrures parentaux.
La variation du degré de saturation-insaturation sexprime:
au départ des hydrures parentaux saturés que
sont les alcanes par le changement de désinence -ane
en -ène ou -yne: butane,
but-1-ène, but-1-yne
De la même manière, on modifie les cycloalcanes en cycloalcènes et
cycloalcynes.
au départ des composés de type MADONC, en
utilisant des préfixes non séparables hydro et déhydro,
avec les préfixes multiplicatifs di-, tétra-, etc.: 1,2-dihydronaphtalène
Notons que le benzène fait exception à ce mode.
|
Préfixes séparables |
préfixes non-séparables (cyclo, déhydro, hydro) |
hydrure parental |
ane ène yne |
suffixes exclusifs |
suffixes cumulatifs (radicaux, cations, anions) |
Finalement, notons que la confection dun nom substitutif est un processus qui se fait par étapes. Chaque étape a son importance, ses règles, ses critères. Il faut franchir ces étapes dans un ordre déterminé de manière à éviter les erreurs, pour aboutir à un nom univoque. Ces étapes sont:
i) la sélection de lhydrure parental, chaîne ou anneau; elle se fait selon des critères de sélection précis, allant du plus simple (par exemple, la chaîne la plus longue dans le cas dun alcane ramifié) au plus complexe (les préfixes non-séparables font parti du nom de lhydrocarbure parental, tétrahydrofurane);
ii) la détermination du degré de saturation-insaturation, selon les deux modes établis;
iii) la détermination des chaînes latérales, groupes caractéristiques, substituants rattachés à lhydrure parental, en particulier du groupe caractéristique principal qui sera désigné par un suffixe (cet ordre des substituants a été établi dans les années 1920 selon labondance des fonctions que lon observait dans ce temps là);
iv) numérotage de lhydrure parental en appliquant la règle des plus petits indices (i.e. les plus petits indices en ordre croissant) et détermination des indices de position de chaque substituant, selon les règles de lUICPA (Il est a noter que lon ne fait pas la somme pour obtenir le plus petit total, mais bien les plus petits possibles. Cette "somme" était une conception fausse et sans fondement...);
v) confection dun nom final, en assemblant le nom de lhydrure parental et ceux des préfixes et suffixes, puis en écrivant un nom complet - en français! (ce qui nest pas de la chimie) -, puis en ajoutant les préfixes multiplicatifs sans modifier lordre orthographique établi précédemment et finalement en ajoutant les indices de position appropriés, les stéréodescripteurs et les modificateurs isotopiques, sil y a lieu (devant les noms auxquels ils sont associés).
Notes
Il existe certains noms conservés, tel iso-propane, néo-pentane, mais on ne les utilise jamais comme hydrure parental.
Il reste dans la nomenclature 153 noms triviaux de base (furane, naphtalène, etc.), ce qui est moins que le nombre dos dans le corps humain, pour nommer les 14 millions de composés existants.
Exemples
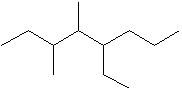 |
5-éthyl-3,4-diméthyloctane |
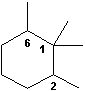 |
1,1,2,6-tétraméthylcyclohexane |
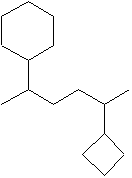 |
2-cyclobutyl-5-cyclohexylhexane |
| trans pent-2-ène | |
| butane -> butène -> butdiène -> butadiène (le a élidé revient ici) -> buta-1,3-diène -> 2-heptylbuta-1,3-diène |
|
| CH2=CH2 | éthène |
| CH2CH2 | éthylène |
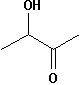 |
3-hydroxybutan-2-one |
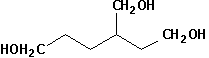 |
3-(hydroxyméthyl)hexane-1,6-diol |
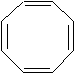 |
cycloocta-1,3,5,7-tétraène (cycle MADONC) |
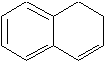 |
1,2-dihydronaphtalène (à cause du préfixe non-séparable dihydro, ce nom est considéré comme un tout et devient un nom dhydrure parental) |
3.2.3. Évolution de la nomenclature et tendances actuelles
Lévolution de la nomenclature se fait en éliminant progressivement les noms triviaux au profit des noms formés systématiquement. Elle se poursuit aussi en favorisant la nomenclature substitutive et en délaissant celle qui fait appel aux noms de classe fonctionnelles; dautre part, la nomenclature par remplacement gagne du terrain.
3.2.4. Les noms triviaux et les noms systématiques
Les chimistes aiment à utiliser des noms simples
, généralement sans indices de position. Ils préfèrent aussi conserver le nom acétone plutôt que dutiliser le nom systématique propan-2-one.Il fut un temps où presque tous les acides gras (aliphatiques) portaient des noms triviaux. Aujourdhui, officiellement, il en reste six dans la série des acides saturés: les acides formique, acétique, propionique, butyrique, palmitique et stéarique. De plus, une différence majeure existe entre ces noms: un seul, lacide acétique, peut être utilisé comme hydrure parental fonctionnalisé, cest-à-dire peut engendrer des noms substitutifs comme par exemple "acide chloroacétique". Les cinq autres noms ne peuvent être utilisés que pour nommer lacide lui-même, non substitué: ainsi, le nom de:
Cl-CH
2-CH2-COOHsera acide 3-chloropropanoïque et non "acide 3-chloropropionique", encore moins "acide
b-chloropropionique".3.2.5. La nomenclature substitutive
Depuis déjà quelques années, la nomenclature substitutive déplace la nomenclature des classes fonctionnelles. On dit ainsi méthanol et éthanol et non plus alcool méthylique et alcool éthylique, iodométhane plutôt que iodure de méthyle. Certains noms, toutefois, ont la vie dure; par exemple loxyde de diéthyle (que lon nomme à tort éther diéthylique ou éther éthylique ou éther tout court) ne cède pas facilement le pas à éthoxyéthane.
La tendance actuelle est aussi dutiliser de plus en plus la nomenclature en -ane généralisée. Cest une nomenclature substitutive qui suit de près celle qui a remporté tant de succès au départ des alcanes. En combinant un préfixe " a " avec la terminaison -ane (identique à celle des alcanes) on obtient les nome des hydrures parentaux des éléments des groupes 14, 15, 16 et 17, plus ceux relatifs au bore et au mercure. La molécule NH
3 est alors lazane, H2S est le sulfane et H2O loxydane. Les noms| tributylazane | (N,N-dibutylbutanamine) |
| diméthylsulfane | (sulfure de diméthyle) |
| diéthyloxydane | (oxyde de diéthyle) |
remplaceront peut-être un jour les noms actuels. Ce type de nomenclature sera peut-être utilisé tous les jours; pour le moment, la plus extrême prudence est de rigueur, car ces noms viennent de voir le jour et nont pas encore subi le test du temps.
3.2.6. La nomenclature par remplacement
Un remplacement se produit, en termes de nomenclature, lorsquun atome (hétéroatome) prend la place du carbone dans une chaîne ou un cycle.
Latome de remplacement est désigné par un préfixe non séparable dit préfixe en " a ": un atome doxygène est désigné par oxa, un atome dazote par aza, etc. Ce type de nomenclature est simple, surtout dans les cas de substitution dissymétrique. Dans les chaînes, il faut toutefois au moins quatre hétéroatomes pour pouvoir utiliser la nomenclature par remplacement.
![]()
2,5,9,12-tétraoxatridécane
ou 1,3-bis(2-méthoxyéthoxy)propane
Cette nomenclature prend de limportance.
Il faut cependant lutiliser avec prudence, car les principes et les règles sous-jacents sont en voie délaboration. Il est tout à fait prématuré dappeler loxyde de diéthyle le " 3-oxapentane ".![]()
3.2.7. "En conclusion
1) changeons ce qui doit être changé;
2) appliquons les principes, règles et critères tels que recommandés par lUICPA;
3) ne précipitons pas lutilisation immédiate et sans discernement des tendances évolutives de la nomenclature; au contraire, préservons notre héritage et notre patrimoine."
Henri Favre, chimiste, 25 novembre 1992
3.2.8. Alphabet grec
|
a, A , alpha |
b, B , bêta |
g, G , gamma |
d, D , delta |
e, E , epsilon |
|
z, Z , zêta |
h, H , êta |
q, Q , thêta |
i, I , iota |
k, K , kappa |
|
l, L , lambda |
m, M , mu |
n, N , nu |
x, X , ksi (xi) |
o, O , omicron |
|
p, P , pi |
r, R , rhô |
s, S , sigma |
t, T , tau |
u, U , upsilon |
|
f, F , phi |
c, C , chi |
y, Y , psi |
w, W , oméga |
3.2.9. Suffixes et préfixes utilisés pour quelque groupes caractéristiques en nomenclature de substitution selon les priorités attribuées aux différentes classes
Le symbole -(C) indique que latome de carbone
appartient à lhydrure parental:
|
Classes de composés |
Formules |
Suffixes |
Préfixes |
|
Acides carboxyliques |
-(C)OOH |
acide -oïque |
|
|
Halogénures dacides |
-COCl |
|
chlorocarbonyl- |
|
Esters |
-COOR |
|
R-oxycarbonyl- |
|
Amides |
-CONH 2-(C)ONH2 |
-carboxamide |
carbamoyl- |
|
Nitriles |
-CN |
-carbonitrile |
cyano- |
|
Aldéhydes |
-CHO |
-carbaldéhyde |
formyl- |
|
Cétones |
=O |
-one |
oxo- |
|
Alcools, phénols |
-OH |
-ol |
hydroxy- |
|
Thiol |
-SH |
-thiol |
sulfanyl- |
|
Hydroperoxydes |
-OOH |
|
hydroperoxy- |
|
Amines |
-NH 2 |
-amine |
amino- |
|
Imines |
=NH |
-imine |
imino- |
|
Éthers |
-OR |
|
R-oxy- |
|
Sulfures |
-SR |
|
R-sulfanyle- |
|
Peroxydes |
-OOR |
|
R-peroxy- |
3.2.10. Groupes substituants toujours désignés par des préfixes
|
Groupes |
Préfixes |
Groupes |
Préfixes |
|
-Br |
bromo- |
-Cl |
chloro- |
|
-ClO |
chlorosyle- |
-ClO2 |
chloryle- |
|
-ClO3 |
perchloryle- |
-F |
fluoro- |
|
-I |
iodo- |
-IO |
iodosyle- |
|
-IO2 |
iodyle- |
=N2 |
diazo- |
|
-N3 |
azido- |
-NO |
nitroso- |
|
-NO2 |
nitro- |
-OR |
R-oxy- |
|
-SR |
R-sulfanyle- |
|
En ce qui concerne la
nomenclature des alcanes proprement dits, létudiant est invité
à réviser le chapitre 1 sur les alcanes dans Favre.
Le tableau 2.4 (p.48 Vollhardt) est aussi intéressant
à consulter. |
3.3. Propriétés physiques des alcanes (Vollhardt 2.4, Arnaud 8-1, 8-3)
Les premiers termes de la série sont des gaz (méthane, Eb=-164°, au butane, Eb=-0,5°). À mesure que le poids moléculaire augmente ils deviennent des liquides (du pentane, Eb=35° jusquà lhexadécane, C
16H34), puis des solides (heptadécane, F=22° et plus). Toutefois, leur point de fusion ne dépasse pas 100° (F=99° pour lhexacontane, C60H122).|
Se référer à la figure 2.3 page 53 (Vollhardt) |
À létat naturel, les alcanes existent en grande quantité dans les gisements naturels de gaz et de pétroles. Ces gisements viennent de la lente fossilisation des divers organismes préhistoriques enfouis. À lexception des premiers termes de la série allant de CH
4 à C6H14, il est impossible disoler les isomères particuliers à cause de leur nombre astronomique. Pour préparer un alcane particulier, il est plus aisé de le préparer artificiellement.Il faut mentionner ici quà masse moléculaire égale, les isomères qui possèdent la structure la plus ramifiée possède le point débullition le plus bas:
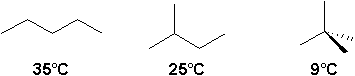
Ceci sexplique par les interactions de Van der Waals et des forces de London. Sans entrer dans les détails, plus une molécule est linéaire, plus elle a la possibilité dinteragir avec ses voisins. Au contraire, plus la molécule est sphérique, moins elle aura de contacts avec ces voisins.
Lintensité et le nombre de ces contacts détermine les propriétés de point de fusion et de point débullition.
Cest aussi pourquoi le point de fusion et débullition augmentent avec le poids moléculaire.|
Démonstration |
Les alcanes sont tous absolument insolubles dans leau.
Toutefois ils servent eux-mêmes de solvants pour les composés organiques non-polaires liquides et solides. Ils servent par exemple de diluants à peinture. On retrouve certains dentre eux sous le vocable déthers de pétrole.3.4. Analyse conformationnelle (Vollhardt 2.5)
Il est important de noter que toutes les façons que nous avons vues de représenter une molécule ne tiennent en aucun compte dun facteur important: ces molécules bougent dans lespace et les liaisons qui unissent deux atomes ne sont pas des tiges rigides immobiles. Il est possible deffectuer des rotations autour de ces liaisons. Les trois groupements liés à un atome de carbone sont alors libres de se retrouver dans toutes les positions possibles.
|
Démonstration de rotation autour de liaisons simples du méthane |
Dans le cas dune molécule comme léthane, cela amène les groupements à prendre des conformations que lon appelle éclipsées et décalées, selon les projection de Newman.
On appelle de telles structures, différentes seulement par la rotation de liaisons simples des isomères de conformations, des conformères ou des rotamères.
En 1935, E. Teller et B. Topley ont suggéré que la rotation observée dans un tel cas pourrait ne pas être totalement libre. Leurs études de la capacité calorifique de léthane ont montré que celle-ci était plus basse que la valeur théorique qui tenait compte seulement de la rotation libre. Ils pensèrent que lon pouvait faire coïncider la théorie et lexpérience à condition que la rotation autour de la liaison CC ne soit pas libre, mais gênée par une barrière dénergie. Dautres études ont montré que cétait aussi le cas pour les liaisons CN et CO.
Cest Derek Barton [Note], en 1950, qui montra la présence de ces conformères et leur effet sur les diverses propriétés physiques et chimiques.
Ces travaux de Barton jetèrent les bases de létude thermodynamique et cinétique de ces conformères et que lon appelle lanalyse conformationnelle.
|
Démonstration des
conformères éclipsés et décalés de léthane |
Dans les conformations éclipsées, des interactions entre les atomes déstabilisent la molécule:
Répulsion de Van der Waals des atomes dhydrogène
Répulsion électrostatique des électrons
Cest pourquoi les conformations décalées sont des conformations de moindre énergie.
Évidemment, cela peut amener des problèmes lorsque certains de ces substituants sont plus gros que dautres. Il en résulte des barrières dénergie inégales. Ainsi, ce ne sont pas tous les conformères qui vont posséder la même probabilité dexistence.
| Ce concept est très important à
retenir pour le reste du cours.
|
Il faut donc se rappeler que les conformères ne sont pas statiques, et que la conversion dune forme dans lautre est très rapide. À température ordinaire (20°C), lénergie cinétique moyenne des molécules gazeuses (kT) vaut environ 0.6 kcalmol-1. Toutefois, comme la répartition des énergies suit la répartition de Boltzmann, il existe des molécules qui possèdent lénergie suffisante pour franchir la barrière dénergie dinterconversion des conformères (voir Fig 2.9 p. 65 Vollhardt).
3.5. Réactivité des alcanes (Arnaud 8-2)
Les liaisons CC et CH étant respectivement non et très peu polarisées, il en résulte que leur rupture est extrêmement difficile. De plus, elles sont très peu polarisables en raison de la faible mobilité des électrons
s. En conséquence, les alcanes présentent une très grande stabilité chimique et sont très peu réactifs. Ils ne sont réactifs que sous des conditions radicalaires, de haute température ou par photochimie. Ils ne sont pas attaqués par les acides forts, ni les oxydants forts ni les réducteurs forts.Cette absence de réactivité des chaînes hydrocarbonées explique que les diverses réactions observées en chimie organique font intervenir des divers groupements fonctionnels.
Toutefois, comme tous les composés organiques, les alcanes sont combustibles, i.e. quils brûlent en présence doxygène et donnent les produits suivants:
2 CnH2n+2 + (3n+1) O2 ® 2n CO2 + (2n+2) H2O
....... DH° = -50 kJg-1Cette réaction nest daucune utilité du point de vue chimique, mais par contre son caractère fortement exothermique explique le très grand intérêt pratique des alcanes comme sources dénergie, soit thermique (centrales au mazout) soit mécanique (moteurs à explosion).
|
|
3.6. Hydrocarbures cycliques (Vollhardt chapitre 4)
Les cycloalcanes sont des alcanes dont une des chaînes est refermée sur elle-même pour former un cycle. Il existe selon une très grande diversité:
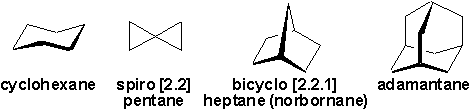
Le nombre minimal datomes de carbones nécessaires pour former un cycle est évidemment de trois (3). Toutefois, il nexiste aucune limite supérieure au nombre datomes dans un cycle.
Les cycloalcanes possèdent la même formule brute que les alcènes: CnH2n.
Les cycloalcènes possèdent la même formule brute que les alcynes: CnH2n-2.
Les cycloalcynes possèdent la même formule brute que les diènes: CnH2n-4.
Du point de vue de la nomenclature, les cycloalcanes forment des radicaux cycloalkyle. lorsque les cycloalcanes portent des substituants sur des carbones différents, ceux-ci peuvent présenter une isomérie cis-trans.
|
En ce qui concerne la nomenclature des
cycloalcanes proprement dits, révisez le chapitre 6.1 dans Favre.
Il est à notre que les structures bicyclo et spiro ne sont pas
les plus usuelles ni les plus importantes. |
3.6.1. Caractères Physiques (Vollhardt 4.1 et Arnaud 11-1)
Les caractères physiques des hydrocarbures cycliques ne présentent pas de différences avec celles rencontrées avec les hydrocarbures acycliques. Les points débullition et les densités sont du même ordre de grandeur, quoiquun peu plus élevés. Ceci est dû aux interactions de London qui seront plus marquées au sein des systèmes cycliques qui sont relativement plus rigides et plus symétriques que les alcanes linéaires. À ce sujet, voir le Tableau 4.1 à la page 109 dans Vollhardt.
3.6.2. Tension de cycle et structure des cycloalcanes (Vollhardt 4.2)
Lorsque lon compare les chaleurs de formation de certains cycloalcanes (Tableau 4.2 Vollhardt p.111) on saperçoit quil existe une énorme différence entre la valeur du
DH°f mesuré et sa valeur théorique. La différence est attribuée à un problème rencontré dans la formation des cycles eux-mêmes. En effet, les premiers termes de la série ne se prêtent pas aux angles de liaison normales. Alors que lon sattend à ce que langle C-C-C soit de 109° environ, on saperçoit quil est impossible de former une molécule comme le cyclopropane.Toutefois, nous savons quune telle molécule existe, et on a même mesuré les angles de liaisons qui sont de 60°. Cest dire que la molécule a la forme dun triangle équilatéral. Lorsque lon brûle cette molécule, elle libère beaucoup plus de chaleur que le propane. Cette énergie supplémentaire vient de la tension accumulée dans le cycle.
En raison de ce profil de tensions, les chimistes organiciens ont schématiquement défini 4 groupes de cycloalcanes:
-
Les petits cycles (C3 et C4) sont extrêmement tendus.
-
Les cycles courants (C5, C6 et C7)
-
Les cycles moyens (C8 à C12)
-
Les grands cycles (C13 et plus) qui sont exempts de toute tension.
Les facteurs responsables de cette tension sont (1) la tension due aux angles de liaison du carbone tétraédrique; (2) la tension déclipse des atomes dhydrogène; (3) les interactions gauches , comme dans le cas du butane et (4) la tension transannulaire des atomes dhydrogène au travers du cycle.
La figure 4.2 (Vollhardt p.112) montre bien le problème rencontré par le cyclopropane (problème de langle inter orbital).
La figure 4.3 (Vollhardt p.112) montre bien le problème rencontré par le cyclobutane (avènement de langle de pliure).
Cet angle de pliure est aussi visible dans le cas du cyclopentane (Vollhardt p.113 en bas) et de sa conformation enveloppe.
3.6.3. Le cyclohexane et les cycloalcanes substitués (Vollhardt 4.3 et 4.4)
Le cyclohexane présente un intérêt particulier. En effet, lanneau cyclohexane est lune des entités structurales les plus abondantes et les plus importante en chimie organique. On en retrouve ses dérivés substitués dans un bon nombre de molécules naturelles et, par ailleurs, la compréhension de sa mobilité conformationnelle constitue un aspect important de la chimie organique.
En effet, si on le représente pas la configuration plane hypothétique on mesure un angle CCC de 120°:
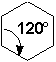
En fait il nen est rien. Rappelez-vous que cette représentation est inexacte car vous tentez de représenter en 2D ce qui est une molécule 3D. La molécule de cyclohexane peut au contraire prendre deux formes particulières que lon nomme forme chaise et forme bateau. Les deux formes sont obtenues en déplaçant les carbones 1 et 4 hors du plan de la coplanéité. Dans le premier cas, en directions opposées, dans le second, du même côté. Il est résulte que la forme chaise se trouve quasiment libre de toute tension (Tableau 4.2 p.111 et Figure 4.5 p.114 Vollhardt).
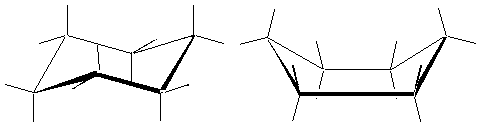
Létudiant est invité à lire avec beaucoup dattention les
paragraphes qui expliquent la façon correcte de dessiner les
conformations chaise du cyclohexane aux pages 116-117.
Lorsque le cyclohexane est dans nimporte laquelle de ces deux configurations, langle C-C-C est très près de 109°. Ainsi, le cyclohexane ne possède presque aucune tension interne. De plus, la molécule peut rapidement sinterconvertir dune forme à lautre avec une faible barrière dénergie de conversion tel que montré à la Figure 4.9 (Vollhardt p.116).
| Démonstration de rotation autour de liaisons simples du cyclohexane |
Toutefois, à cause du nombre de liaisons éclipsées (8) quelle contient, la forme bateau est moins stable que la forme chaise, qui ne contient que des conformations éclipsées. En fait, léquilibre est de 99%+ en faveur de la forme chaise. Cette forme bateau nexiste pratiquement que dans des cas spéciaux lorsque dautres atomes forment un pont interne comme dans le norbornane (bicyclo[2.2.1]heptane)
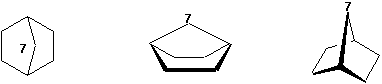
Un autre fait intéressant du cyclohexane est quil existe en fait une multitude de formes chaises. Lors de chaque interconversion, les liaisons équatoriales deviennent axiales et vice versa. cela permet de stabiliser la molécule lorsquelle contient des groupements volumineux (Figures 4.10, 4.11, 4.12, Vollhardt p. 116 à 119, de même que la figure du haut de la p.121). Cest ce qui explique plusieurs des propriétés des cycles à 6 atomes que nous verrons plus tard dans ce cours.
Par exemple, calculons la probabilité de retrouver des deux formes du méthylcyclohexane. Celui-ci présente 2 interactions gauches lorsque le groupement méthyle est en position axiale, alors que ces interactions sont anti lorsque le méthyle se retrouve en position équatoriale. Les autres interactions étant les identiques, on calcule ainsi quil y a une différence dénergie de 1.6 kcalmol
-1 en faveur de la conformation équatoriale. À laide de la relation: DG = -RT ln K on évalue léquilibre à température de la pièce comme contenant 93% de forme équatoriale et 7% de forme axiale.| Démonstration de rotation autour de
liaisons simples à laide dun modèle moléculaire méthylcyclohexane
ou de 1,3,5-trichlorocyclohexane Démonstration de rotation autour de liaisons simples à laide dun modèle moléculaire cis-1-(1,1-diméthyléthyl)-2-méthylcyclohexane (faire ici lexercice de nomenclature) |
3.6.4. Les cycloalcanes supérieurs (Vollhardt 4.5)
Comme la montré le Tableau 4.2 (Vollhardt p.111) les cycles contenant 8 à 12 membres présentent à nouveau des tensions, principalement à cause de la distorsion des liaisons et des interactions transannulaires. Ceci est clairement montré pour les cycloheptane, cyclooctane et cyclodécane à la page 130 dans Vollhardt.
Ainsi, la conformation adoptée par les cycles représente un compromis entre les facteurs responsables de cette tension qui sont rappelons-le:
- la tension due aux angles de liaison
- la tension déclipse
- les interactions gauches
- la tension transannulaire
Les cycles moyens sont difficiles à synthétiser et très rares.
La tension diminue beaucoup et disparaît presque dans les grands cycles. Ils adoptent une conformation comprenant deux longues chaînes parallèles de configuration tout-anti reliées par des segments courts.
3.6.5. Les alcanes polycycliques (Vollhardt 4.6)
Lorsque deux cycles ont en commun deux atomes de carbone adjacents, comme dans le cas de la décaline, on dit que ces deux cycles cyclohexanes sont fusionnés, ou encore annelés (voir Vollhardt p.123 en haut). Les composés de ce type sont appelés des bicycliques. Ils sont caractérisés par deux atomes de carbone, les carbones têtes de pont, qui sont partagés par deux cycles.
Ces molécules sont nommées systématiquement en tant que dérivés du cycloalcane contenant le même nombre de carbones annulaires. Le nom est précédé par le préfixe bicyclo (voir Favre 6.1.2). On indique ainsi la longueur des ponts (le # datomes de carbones qui les composent). Voici le système de numérotation utilisé:
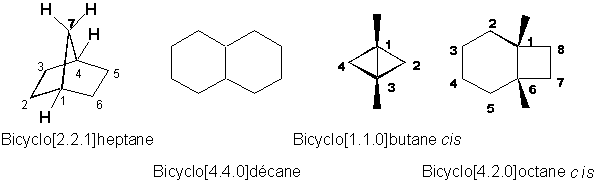
Enfin, les cycloalcanes peuvent être fusionnés en cis ou en trans. La Figure 4.13 (Vollhardt p.123) montre lexemple des deux isomères du bicyclo[4.4.0]décane.
Quelle est la limite des hydrocarbures tendus, nul ne le sait! Citons ici les exemples du cubane (1964), du tétrakis(1,1-diméthyléthyl)tétraédrane (1978), du dodécaédrane (1982). Ce dernier possède un point de fusion de 430°C, alors que leicosane (C20H42) possède un point de fusion de 36,8°C!
Enfin, mentionnons que le motif cyclohexanique en forme chaise se retrouve dans de nombreuses molécules organiques et des réseaux cristallins inorganiques, comme le diamantane et le diamant respectivement.
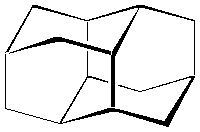 Diamantane
Diamantane
Enfin, il ne faut pas oublier la classe de composés cycliques appelés spiroalcanes. Au lieu davoir deux atomes de carbone comme tête de ponts, ceux-ci possèdent un atome de carbone commun à deux cycles. Il va de soit quil sagit ici dun carbone de type quaternaire. Leur structure et nomenclature est expliquée dans le chapitre 6.1.3 dans Favre.
3.6.6. Les produits naturels cycliques (Vollhardt 4.7)
On retrouve de nombreux composés cycliques dans les produits naturel.
Plus spécialement dans les produits de la classe des terpènes et des stéroïdes sur lesquels nous reviendrons plus tard dans le chapitre 10.3.6.7. Réactivité (Arnaud 11-2)
En ce qui concerne leur réactivité, les hydrocarbures cycliques ne présentent pas de différences notables avec celles rencontrées avec les hydrocarbures acycliques.
Par contre, à cause des tensions introduites dans les petits cycles, comme le cyclopropane par exemple, ces cycles tendent à souvrir par rupture dune liaison carbone-carbone. Cest particulièrement évident dans le cas de la combustion. Ces cycles libèrent plus dénergie en brûlant que ce à quoi on pourrait sattendre. Cela est facilement expliqué par la tension qui existe dans certains cycles. Cette tension représente une énergie supplémentaire qui est libérée par la combustion.
3.6.8. État naturel (Arnaud 11-3)
Des cycloalcanes sont présents dans certains pétroles, notamment dans les gisements dEurope centrale. Diverses essences végétales contiennent des hydrocarbures cycliques non saturés, mono- ou polycycliques comme le limonène (citron) et le pinène (résine de pin).
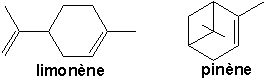
Mais il est plus fréquent de trouver dans la nature des molécules cycliques, couvent polycycliques, comportant en outre des fonctions diverses comme alcool, aldéhyde, cétone, acide (mais évidemment nous ne parlons plus ici dhydrocarbures). On peut mentionner ici la série des stéroïdes: cholestérol, cortisone, hormones sexuelles.
| Létudiant est invité à lire la section 4.7, mais
celle-ci ne sera pas matière à examen avant que nous ayons vu le
chapitre 10. Encart du chapitre 4 Notions importantes dans Vollhardt aux pages 128 et 129. Tous les problèmes (sauf 3, 4, 6, 9, 14b, 15 à 18, 21d, 22 à 24) des pages 129 à 135 peuvent être faits. |
3.7 Erratum du livre "Les Fondements de la Nomenclatue de la Chimie Organique"
Suite à un échange avec lauteur, voici quelques modifications, ajouts, et coquilles à corriger dans la deuxième édition (1996) de louvrage.
"La nomenclature, jusquà ce jour, avait pour but dêtre non ambigüe. De là, un certain nombre de noms pour le même composé de façon à ne déplaire à personne. Il y a des traditions liées aux langues, aux sociétés savantes, à certains types dindustrie et surtout aux individus qui ne veulent pas démordre dune certaine façon de faire. De là une confusion certaine et le projet actuel de lUICPA de ne retenir quun nom, le seul préféré. Les résultats de ce projet seront publiés en 1998 ou 1999."
(Henri Favre, 13 novembre 1996)p.30 - Tableau III. Lordre de priorité des classes fut déterminé par labondance de lensemble des composés connus il y a une centaine dannée. Les acides étaient fort nombreux en raison de la facilité avec laquelle on pouvait les isoler et les purifier. Les amines, comme encore aujourdhui dailleurs. étaient difficiles daccès. Savez-vous que la dessinence -ane signifiait la saturation et les autres, dans lordre alphabétique, linsaturation: -ène, double liaison, -ine, triple liaison? La situation sest gâtée quand les quadruples et quintuples liaisons ne se sont pas matérialisées. La dessinence -ine est, aujourdhui, réservée aux amines, -one aux cétones, -yne aux acétyléniques et -une vient dêtre proposée pour décrire une situation provisoire lorsquon ne connait pas le groupe caractéristique principal. On évitera ainsi de nommer prostaglandine le composé dépourvu dazote qui est en fait un acide carboxylique.
p.36 - 4,4-bipyridine sera le seul nom accepté
p.59-60 - Méthanamine, N-méthylméthanamine et N,N-diméthylméthanamine (méthylazane est à bannir)
p.61 - Le composé doit être nommé N, N, N"-triméthylpropane-1,2,3-triamine et non N, N, N"-triméthylbutane-1,2,3-triamine
p.79 - Le composé doit être nommé 2,3-diméthylspiro[5.5]undéc-1-ène
p.92 - Au milieu: la structure du composé 2H-furo[3,2-b]pyrane doit en fait être:
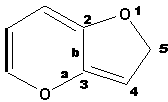
p.92 - Au milieu à droite: enlever un [
p.110 - En suivant les exemples, le nom de lester suivant serait (section 5.8.1 pour le groupe acétoxy): acide 4-acétoxycyclohexane-1-carboxylique
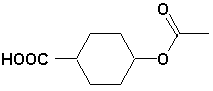
p.165 - Corrigez les formules pour les suivantes
1,4-dioxane-1,4-diium 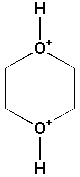 et pyridinium
et pyridinium 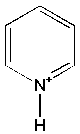
p.176 - Le composé doit être nommé r-1,c-2,c-3,c-4-pentaméthylcyclobutane
p.176 - Le composé doit être nommé c-4-isopropyl-c-2-méthylcyclohexan-r-1-ol
p.176 - Le bomposé dibromé: remplacer B
p.178 - Il manque un ï sur le nom de lacide icosatétraénoïque
3.8 Exercices de nomenclature
La confection dun nom substitutif est un processus qui se fait par étapes. Chaque étape a son importance, ses règles, ses critères. Il faut franchir ces étapes dans un ordre déterminé de manière à éviter les erreurs, pour aboutir à un nom univoque. Dans un composé acyclique, la chaîne sur laquelle sont basés la nomenclature et le numérotage est appelée "chaîne principale". Quand on doit choisir la chaîne principale dans un composé acyclique, on applique les critères ci-après, dans lordre indiqué, jusquà ce quune solution intervienne.
a) nombre maximal de substituants correspondant au groupe principal
b) nombre maximal de doubles et triples considérées dans leur ensemble
c) longueur maximale
d) nombre maximal de doubles liaisons
e) plus petits indices de position pour les groupes principaux (notez ici que les liaisons multiples ne comptent pas pour des groupes principaux)
f) plus petits indices de position pour les liaisons multiples
g) plus petits indices de position pour les liaisons doubles
h) nombre maximal de substituants désignés par des préfixes
i) plus petits indices de position pour tous les substituants énoncés en premier dans lordre alphabétique
j) nombre maximal de substituants énoncés en premier dans lordre alphabétique
k) plus petits indices de position pour les substituants désignés par des préfixes et énoncés en premier dans lordre alphabétique
Confection dun nom final, en assemblant le nom de lhydrure parental et ceux des préfixes et suffixes, puis en écrivant un nom complet en français! On ajoute les préfixes multiplicatifs sans modifier lordre orthographique établi précédemment et finalement on ajoute les indices de position appropriés, les stéréodescripteurs et les modificateurs isotopiques, sil y a lieu.
Exemple d'éclaircissement sur la nomenclature
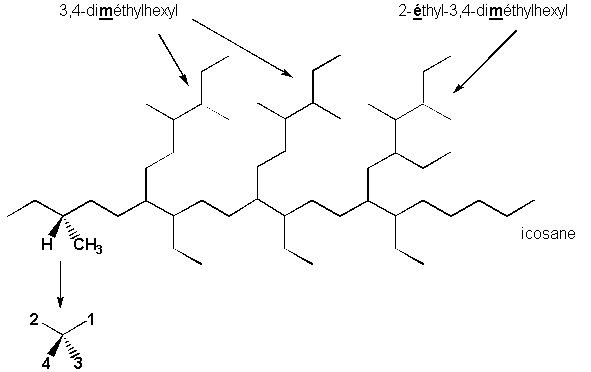
(3R)-6,10-bis(3,4-diméthylhexyl)-7,9,15-triéthyl-14-(2-éthyl-3,4-diméthylhexyl)-3-méthylicosane
Faire les exercices de nomenclature qui sont présentés dans Favre
Autres exemples: (réponses après les structures)
a) 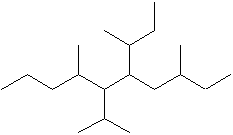 |
b) CH3CH2(CH2)8CH2CH3 |
c) 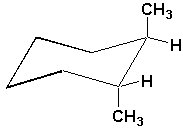 |
d) 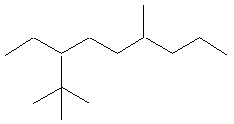 |
e) 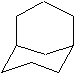 |
f) 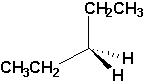 |
g) 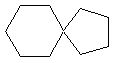 |
h) 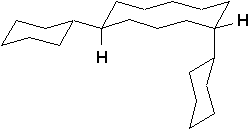 |
i) 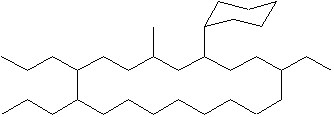 |
Réponses:
a) 3,7-diméthyl-6-(1-méthyléthyl)-5-(1-méthylpropyl)décane
5-sec-butyl-6-isopropyl-3,7-diméthyldécane
(voir 2°:p.11, 1°:p.9)
b) dodécane
c) trans 1,2-diméthylcyclohexane
d) 3-éthyl-2,2,6-triméthylnonane (préféré, règle
UICPA-13.11h)
3-tert-butyl-6-méthylnonane
e) bicyclo[3.3.1]nonane
f) pentane
g) spiro[4.5]décane
h) trans 1,5-dicyclohexylcyclodécane
i) 7-cyclohexyl-10-éthyl-5-méthyl-1,2-dipropylcyclooctadécane
| Retour au menu |
|
ABCSITE © copyright 2000 |