abcsite.free.fr
![]()
Chimie Organique
|
|
1. Introduction
|
Dans ce chapitre |
|
|
1.1. |
|
1.1. Les origines de la chimie organique. (Vollhardt 1.1 +)
En tant quoutil important pour nous permettre daccéder à la connaissance du monde qui nous entoure, la chimie létude de la matière et des règles qui régissent les changements qu'elle effectue sest développée lentement jusque vers la fin du XVIIIe siècle. À cette époque, en se basant sur ses études du phénomène de la combustion, Antoine-Laurent de Lavoisier [Note] apporta des indices que les compositions chimiques pouvaient être déterminées par lidentification et la mesure des quantités deau, de dioxyde de carbone et dautres matières produites lorsque les substances sont brûlées dans lair. À cette époque, la science de la chimie comportait déjà deux grandes divisions: lune traitant des substances obtenues des sources naturelles ou vivantes, et lautre traitant des substances dérivées de la matière non vivante. Il sagissait respectivement de la chimie organique et de la chimie inorganique. Les études de la combustion ont rapidement établies que les composés dérivés de sources naturelles comportaient toujours du carbone. Ceci a amené une nouvelle définition de la chimie organique: létude des composés du carbone. Cette définition est encore utilisée aujourdhui.
Lhistoire de la chimie est fascinante. Pour les gens intéressés, dexcellents ouvrages existent. Parmi les ouvrages que lon retrouve à lUQTR, il est intéressant de consulter:
A history of chemistry / by F.J. Moore (QD11M66)
Histoire de la chimie / Bernard Vidal (AC20Q84V35)
Histoire de la chimie / G. Lockemann (QD11L63F)
Lhistoire de la chimie en bande dessinee / [ill. de] Cinzia Ghigliano ; [texte de] Luca Novelli (QD11G55F)
Lavoisier, theoricien et experimentateur / Maurice Daumas (QD22L4D38)
Les domaines actuels de la chimie sont les suivants: chimie analytique, biochimie, chimie inorganique, nucléaire, organique, physique, chimie de polymères, chimie théorique.
Les molécules organiques constituent lessence même de la vie. Les protéines, les acides nucléiques, les sucres et les graisses sont des composés dont le constituant principal est le carbone. Les vêtements que nous portons sont faits de polymères naturels (coton, soie) ou synthétiques (polyesters). Les produits domestiques dusage courants, dentifrices, savons, shampooings, déodorants, parfums sont tous des produits de lindustrie chimique organique. On peut y inclure aussi les peintures, plastiques, aliments, etc. Il ne faut pas oublier aussi toute la panoplie de produits pharmaceutiques (médicaments, vaccins, antibiotiques) et autres insecticides et pesticides.
1.1.1. Les éléments constitutifs des molécules organiques (Arnaud 1.2)
Les éléments constitutifs des molécules organiques sont, par ordre de fréquence décroissant:
les quatre éléments, C, H, O, N
des non-métaux tels que Cl, Br, I, S, P, As, ...
des métaux tels que Na, Li, Mg, Zn, Fe, Co, Cu, Cd, Pb, Sn, ...
Comment compare-t-on labondance relative de ces éléments par rapport à ce que lon retrouve dans lunivers?
Doù ces éléments viennent-ils? Sans entrer dans les détails cosmologiques, on peut simplifier en disant que lors du Big Bang, lunivers formé contenait environ 93% H et 7% He. Les nuages dhydrogène se sont agrégés et ont formé la première génération détoiles. Les fournaises stellaires ont engendré les éléments plus lourds pour générer les éléments jusquau Fe. Ceci constitue une impasse thermodynamique et certaines étoiles, privées de leur carburant se sont alors effondrées et ont explosé (supernovæ) pour former les autres éléments au-dessus du fer.
|
Univers |
Terre |
Corps Humain |
|||
|
H |
93 |
O, oxydes et eau |
50 |
O, eau, protéines, phosphate |
65 |
|
He |
6.9 |
Si, silicates |
26 |
C |
18 |
|
O |
0.0005 |
Al |
7 |
H, eau |
10 |
|
C |
0.00008 |
Fe |
4 |
N |
3 |
|
N |
0.00015 |
Ca |
3 |
Ca |
2 |
|
Ne |
0.0002 |
Na |
2.5 |
P |
1 |
|
Autres |
0.1 |
K |
2.5 |
K |
0.35 |
|
|
|
Mg |
2 |
S |
0.25 |
|
|
|
H |
0.88 |
Na |
0.15 |
|
|
|
C |
0.087 |
Cl |
0.015 |
|
|
|
N |
0.030 |
Autres |
0.1 |
|
|
|
Autres |
2 |
|
|
Ainsi, à part loxygène qui est très abondant dans la croûte terrestre et le corps humain, les éléments C, H et N, qui constituent 31% du corps humain ne constituent que 1,78% des éléments présents dans lécorce terrestre et moins de 0,1% du total des éléments présents dans lunivers. Tout ceci implique que la chimie organique fait intervenir une très faible proportion des éléments connus.
Passons maintenant une très courte revue historique de la chimie organique.
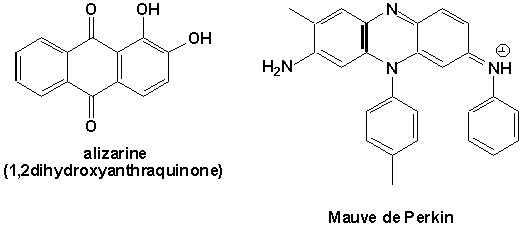
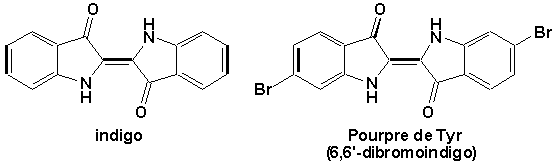
Dès lantiquité, les égyptiens, romains et phéniciens faisaient déjà de la chimie organique en réussissant à extraire des colorants naturels pour sen servir comme éléments de teintures pour leur vêtements. Citons notamment lindigo et lalizarine (provenant de la garance, une plante herbacée aux racines rougeâtre) et la pourpre de Tyr (provenant de coquillages) [Note]. L'industrie chimique organique origine des travaux de Perkin [Note] et de sa découverte du premier colorant synthétique: le Mauve de Perkins.
Des travaux importants ont été effectués dès 1923 par un savant russe du nom de A .I. Oparine [Note] ont portés sur latmosphère primitive de la terre. Il a ainsi proposé que celle-ci était composée dun mélange de H2O / CO2 / N2 / NH3 / CH4. Ceci a conduit Stanley L. Miller [Note] en 1950 a sa fameuse expérience où il a fait passer des décharges électriques dans un ballon contenant un tel mélange gazeux et ainsi former des acides aminés. Ce résultat fut extrêmement important car les protéines, des constituants majeurs des organismes vivants, sont faits dassemblages dacides aminés [Note].
1.1.2. Structure des molécules organiques (Arnaud, 0.4)
Les composés organiques et minéraux et leurs réactions chimiques respectives démontrent des particularités intéressantes. De plus, la position médiane du carbone dans la classification périodique des éléments et dans léchelle des électronégativités a pour conséquence que la chimie organique est essentiellement une chimie de composés covalents possédant des liaisons peu ou non polarisées.
|
Les Composés Organiques |
Les Composés Minéraux |
|
Sont formés de liaisons covalentes, ou à caractère covalent dominant |
Sont formés de liaisons ioniques, ou à caractère ioniques dominant |
|
Sont rarement solubles dans leau, et encore plus rarement des électrolytes |
Sont souvent des électrolytes, solubles dans leau |
|
Ont souvent des points de fusion et débullition bas, beaucoup sont des liquides à la température ordinaire |
Ont souvent des points de fusion et débullition élevés, beaucoup sont des solides cristallisés à la température ordinaire |
|
Ont le plus souvent une masse volumique voisine de lunité |
Ont des masses volumiques variables et souvent grandes (métaux) |
|
Sont facilement décomposé par la chaleur; peu résistants à une température supérieure à 500 °C |
Ont généralement une grande stabilité thermique (matériaux réfractaires) |
|
Sont presque tous des combustibles |
Sont rarement combustibles |
|
Les Réactions Organiques |
Les Réactions Minérales |
|
Sont souvent lentes, réversibles et incomplètes |
Sont souvent rapides et totales |
|
Ont le plus souvent des effets thermiques faibles (faible différence dénergie entre état initial et état final) |
Ont le plus souvent des effets thermiques forts (exothermiques ou endothermiques) |
1.1.3. Pourquoi le carbone? (Allinger 1)
Le carbone possède une configuration électronique 1s22s2p2 et donc 4 électrons de valence sur sa couche externe. ceci implique quil aura la possibilité de former jusquà 4 liens covalents pour compléter sa couche externe à 8 électrons (règle de loctet). La chimie particulière du carbone résulte de sa capacité à hybrider ses orbitales (on y reviendra sous peu).
Il est intéressant de noter quà cause de leur électronégativités voisines, les éléments N, H et O peuvent former des liaisons covalentes avec le carbone.
Accessoirement, on peut se demander si une chimie du même type que celle que lon observe avec le carbone est possible avec dautres éléments, notamment le silicium qui partage de nombreuses affinités électroniques avec le carbone: C [1s22s2p2] vs Si [1s22s2p63s2p2]. il faut ici regarder la force des diverses liaisons en jeux:
|
Lien |
kJmol -1 |
Lien |
kJmol -1 |
|
C-C |
610 |
C-H |
337 |
|
Si-Si |
327 |
C-O |
1077 |
|
Ge-Ge |
274 |
C-N |
770 |
|
Sn-Sn |
195 |
O-H |
428 |
|
Pb-Pb |
340 |
H-H |
436 |
|
O-O |
499 |
Si-O |
799 |
|
|
|
Si-H |
299 |
Ainsi, lénergie de liaisons de Si-O et C-C sont plus fortes que celles présentées par Si-Si. Ceci explique pourquoi les chaînes Si-Si sont détruites dans une atmosphère oxydante. Ainsi, les autres formes de vie que lon voit dans les films de science-fiction ne peuvent exister dans une atmosphère oxydante comme celle que nous possédons.
| Retour au menu |
|
ABCSITE © copyright 2000 |