abcsite.free.fr
![]()
Chimie Organique
|
|
7. Hydrocarbures insaturés
|
Dans ce chapitre |
|
| 7.1. | Les alcènes |
| 7.2. | Diènes, allènes, diènes conjugués et polyènes |
| 7.3. | Ordre de liaison p |
| 7.4. | Termes importants et utilisations |
| 7.5. | Les alcynes |
| 7.6. | Sites dinsaturation |
| 7.7. | Exercices de nomenclature |
| Modèles Moléculaires en format .pdb: Alcènes et alcynes | |
7.1. Les alcènes (Vollhardt chapitre 11)
La double liaison carbone-carbone est le groupe fonctionnel des alcènes. Anciennement, cette classe de composés était appelée oléfines (oleum, latin huile; facere, latin, faire). Ce nom apparut parce que de nombreux alcènes donnent naissances à des huiles lors des réactions daddition sur les doubles liaisons.
On les appelle également hydrocarbures éthyléniques, du nom du premier terme de la série, léthylène:
H2C=CH2
Les liaisons doubles C=C sont très fréquentes dans les composés naturels. La réactivité de cette double liaison est caractéristique de tous les alcènes.
Les alcènes de 4 carbones et moins sont gazeux. Pour les autres, le point de fusion et débullition augmente avec le poids moléculaire. Toutefois, à nombre égal datomes de carbone, les alcènes possèdent un point débullition plus bas que les alcanes parce quils sont plus ramifiés (moins dinteractions de van der Waals)
Les alcènes sont insolubles dans leau, mais solubles dans les hydrocarbures.
Les alcènes possèdent la même formule brute que les cycloalcanes: CnH2n.
7.1.1. Nomenclature (Vollhardt 11.1)
La nomenclature des alcènes seffectue en changeant la dessinence -ane en -ène. De plus, à partir de C4, un indice de position est requis pour caractériser la position de la double liaison. On utilise lindice de position le plus petit des deux carbones impliqués dans la double liaison.
Combien disomères possibles du butène existe-t-il? On peut facilement imaginer:
| but-1-ène | CH3CH2CH=CH2 |
| but-2-ène | CH3CH=CHCH3 |
| 2-méthylpropène | (CH3)2C=CH2 |
Toutefois, expérimentalement on découvre quil existe 4 isomères possédant des propriétés différentes. Pourquoi? Parce que la double liaison implique que les 6 atomes impliqués sont coplanaires. Ainsi, le but-2-ène peut se présenter sous la forme de deux isomères géométriques différents, deux diastéréoisomères (on peut envisager la double liaison comme un cycle à deux atomes):
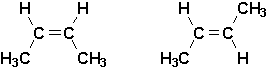
De plus, à cause de la rigidité de la double liaison qui empêche la rotation libre sur laxe carbone-carbone, les substituants sur les carbones impliqués dans la double liaison peuvent se retrouver dans la configuration cis ou trans. Étant donné quil est difficile dattribuer de façon non ambiguë les conformations cis et trans lorsque les atomes de carbones de la double liaison ne portent pas dhydrogène, on utilise le système E, Z du lUICPA.
Celui-ci est basé sur le système Cahn-Ingold-Prelog qui est couramment utilisé pour les notations stéréochimiques. Si les deux groupements prioritaires sont situés de côtés opposés par rapport à la double liaison, la molécule possède la conformation E (de entgegen, allemand, opposé). Dans le cas contraire, i.e. les deux groupements prioritaires sont situés du même côté par rapport à la double liaison, la molécule a la conformation Z (de zusammen, allemand, ensemble).
À ce sujet, voir le chapitre 2 et la section 12.1 dans Favre. Toutefois, lire attentivement les règles 1 à 7 dans Vollhardt p.373 à 376.
Ainsi, nommez les molécules suivantes (Exercice 11.3, Vollhardt p.375) (le problème est de savoir quels groupements considérer en cis et trans):

Notons aussi quil existe 6 alcènes de formule C5H10, alors quil nexiste que 3 alcanes de formule C5H12. Il existera toujours un plus grand nombre disomères pour les alcènes que pour les alcanes correspondants de même nombre datomes de carbone.
7.1.2. La liaison double carbone-carbone (Vollhardt 11.2)
Tel que mentionné alors que nous parlions dhybridation, le carbone éthylénique (portant une liaison double et 2 liaisons simples) est hybridé en sp2. La liaison
p est crée par le recouvrement latéral des orbitales p (Figure 11.1, 11.2, 11.3, Vollhardt p.377-8).Ces deux types de liaisons différentes qui constituent le liaison double,
s et p, vont expliquer la force de la liaison totale. Il est important de noter que lénergie dune double liaison nest pas la somme de lénergie de 2 liaisons simples.À cause du recouvrement moindre des orbitales atomiques p qui constituent lorbitale moléculaire
p, par rapport au recouvrement résultant dans lorbitale moléculaire s, les liaisons p seront plus faibles que les orbitales s (Figure 11.4, Vollhardt p.379). Par isomérisation thermique dune molécule comme le 1,2-dideutéroéthène, on peut mesurer la valeur de lénergie p de la double liaison (Figure 11.5, Vollhardt p.379). On a ainsi calculer quelle est environ de 65 kcalmol-1, alors que lénergie associée à la liaison s est denviron 108 kcalmol-1 (Figure 11.6, Vollhardt p.380).Il en résulte que les réactions subies par les doubles liaisons sont surtout sur cette double liaison
p qui est un site de forte densité électronique dont les électrons sont facilement accessibles car à cet endroit la molécule est plane. Les alcènes seront donc susceptibles aux attaques des réactifs électrophiles. Cest donc un maillon faible dans une chaîne hydrocarbonée et la molécule peut se briser plus aisément à cet endroit.Contrairement aux liaisons simples, les liaisons doubles présentent une rigidité qui empêche la libre rotation autour de laxe carbone-carbone. Les angles de liaisons des deux atomes de carbones étant, rappelons-le, de 120°, toutes les liaisons entourant une liaison double carbone-carbone se retrouvent donc dans un même plan. Regardons ainsi se qui se passe avec une molécule comme le (E)-pent-2-ène (Figure en haut de la p.380).
Cela implique que les deux isomères suivants posséderont des propriétés physiques et chimiques différentes, parce que les groupements sont ici fixés de part et dautre le la liaison double. On ne peut pas effectuer une interconversion cis-trans dans briser la liaison chimique. De plus, on observe la présence dun moment dipolaire dans ces molécules car les atomes hybridés en sp2 sont plus plus polaires à cause du caractère s accru. Il en résulte un moment dipolaire net relativement important dans le cas des alcènes disubstitués en cis, et un moment dipolaire net presque nul dans le cas des alcènes disubstitués en trans.
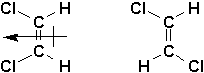
Enfin, il est toujours possible de faire passer un plan de symétrie dans le plan de la double liaison. En effet, on peut séparer des atomes de deux dans de tels plans imaginaires. Il en résulte que les carbone éthyléniques ne sont jamais asymétriques. Imaginez la double liaison comme étant 2 substituants identiques.
7.1.3. RMN des alcènes (Vollhardt 11.3)
Les alcènes possèdent des signatures tout à fait caractéristiques tant en RMN-1H quen RMN-13C. Les hydrogènes alcéniques terminaux (RRC=CH2) apparaissent vers 4.6 à 5.0 ppm, alors que les hydrogènes internes (RCH=CHR) apparaissent vers 5.2 à 5.7 ppm (Tableaux 10.2 et 10.6, Figure 11.7 p.381).
Doù provient ce déblindage prononcé? Ce sont les électrons de la liaison
p eux-mêmes qui, mis en mouvement par Ho créent un champ local qui sajoute au champ externe (Figure 11.9, Vollhardt p.382). De plus, les carbones hybridés en sp2 sont plus électronégatifs que les carbones hybridés en sp3.Il est aussi notable que le couplage des hydrogènes au travers de la double liaison est différent dans le cas des hydrogènes cis et trans. Les constantes de couplage vicinal sont alors Jcis = 9 Hz et Jtrans = 14 Hz. Voir la Figure 11.10 et le Tableau 11.1 (Vollhardt p.383-5). Il peut toutefois en résulter de grandes complexité des profils de couplage tel que montré à la Figure 11.11 (Vollhardt p.384).
Le cas des RMN-13C est aussi très révélateur. Les carbones alcéniques sont déblindés denviron 100 ppm par rapport aux carbones des alcanes correspondants.
7.1.4. Réactivité (Vollhardt 11.7 et Arnaud 9-2)
La stabilité chimique des alcènes dépend de la position de la double liaison à lintérieur de la molécule. Lisomère dans lequel cette double liaison est entouré du plus grand nombre de groupes alkyles (i.e. celui dont la double liaison est la plus substituée) est le plus stable.
Par ailleurs, de deux stéréoisomères possibles, celui dont les substituants les plus encombrants sont placés en trans sont plus stables que ceux ou ils sont placés en cis.
Lordre de stabilité relative des alcènes est le suivant (les hydrogènes ne sont pas montrés par souci de clarté):
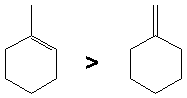
Exemples: méthylbutènes
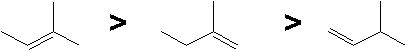
But-2-ène Z et E et méthylcyclohexène vs méthylènecyclohexane
![]()
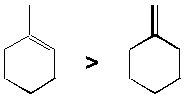
7.1.5. Cycloalcènes (Allinger 7.7)
Les cycloalcènes possèdent la formule générale suivante: CnH2n-2.
En voici quelques exemples:
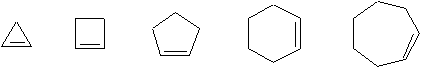
Les cyclopropène et cyclobutène sont des molécules planes extrêmement tendues. Que lon se rappelle la discussion sur le cyclopropane et le cyclobutane, et que lon considère lhybridation qui est sp2 plutôt que sp3. Lon comprendra alors que la tension soit supérieurs à cause des angles dhybridation.
Le cyclopentène est presque plan, alors que les cycles supérieurs ne le sont pas.
Prenons lexemple du cyclohexène. Les carbones 1-2-3-6 sont dans un même plan (parce que C1 et C2 sont hybridés en sp2). Il en résulte que C4 et C5 doivent être soit au-dessus, soit au-dessous du plan pour que leurs angles de liaisons (sp3) soient le plus près de la normale. La structure la plus stable du cyclohexène sera une conformation quasi-chaise:
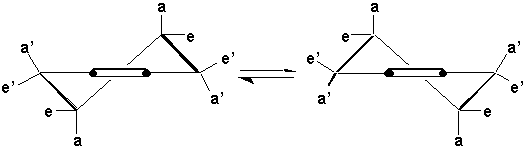
ou a et e sont des substituants pseudo-axiaux et pseudo-équatoriaux.
Les cycloalcènes de 3 à 7 atomes dans le cycle nexistent que sous la forme cis. Le plus petit cycloalcène trans et non substitué isolé est le trans cyclooctène. Il est moins stable que lisomère cis par 9.2 kcalmol-1. Sa structure nest pas plane, mais fortement tordue. De plus, la molécule existe selon deux images spéculaires, deux énantiomères optiquement actifs:
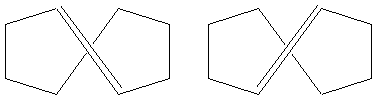
La barrière dinterconversion qui fait intervenir un basculement du cycle est très élevée, environ 36 kcalmol-1.
On peut voir ici un des premiers exemples dactivité optique causé par une rotation empêchée autour de liaisons simples.
7.1.6. Pouvoir électrodonneur des liaisons doubles (Allinger 7.17)
À cause de la géométrie des liaisons
p, les électrons qui la forment sont accessibles. La liaison p joue le rôle dun donneur délectrons, i.e. une base de Lewis. On a même isolé des complexes stables entre les alcènes et des électrophiles. On les appelle des complexes-p, ou complexes de transfert de charge.Il est impossible de décrire ces complexes
p avec des structures de valence classiques. On les représente comme: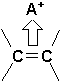
Par exemple: liode en solution aqueuse ou éthanolique est de couleur pourpre. La solution diode dans le cyclohexène est brune:
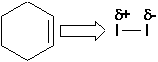
Lion Ag
+ est connu pour ses complexes p avec de nombreux alcènes, surtout avec les diènes conjugués. Le sel ainsi formé est soluble dans leau. On en extrait ensuite lalcène par lajout de NH4OH pour obtenir le très stable complexe [Ag(NH3)4]+ et ainsi libérer lalcène qui sortira de la phase aqueuse.Les alcènes jouent aussi le rôle de ligands dans les complexes de coordination avec les métaux. Ils sont ainsi très importants en catalyse.
Citons le butadiènedichloropaladium et le Ferrocène, bis(cyclopentadiényl)fer
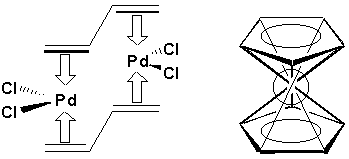
7.1.7. Polymérisation (Vollhardt 12.13 et Arnaud 9-C)
Une polymérisation est une réaction dans laquelle les molécules dun composé se soudent les unes aux autres, en nombre parfois très grand, sans aucune élimination, pour donner une substance (le polymère) dont le poids moléculaire est un multiple exact de celle du composé initial (le monomère).
Par exemple, léthylène peut se polymériser en chaînes linéaires saturées très longues constituant le polyéthylène.
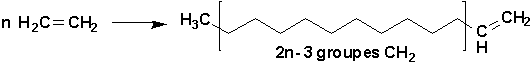
Divers dérivés vinyliques A-CH=CH
2 peuvent également polymériser selon le schéma suivant pour donner une foule de produits que lon appelle les matières plastiques: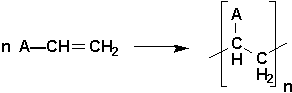
Par exemple:
Le chloroéthène (incorrectement appelé chlorure de vinyle), ClCH=CH2 donne les chlorures de polyvinyle
Lacrylonitrile, H2C=CHC
Le styrène, C6H5CH=CH2, donne les polystyrènes
7.1.8. État naturel (Arnaud 9-3)
Bien que la double liaison C=C soit très fréquente dans les composés naturels, les alcènes purs sont relativement rares dans la nature. Le pétrole nen contient pas. Seulement certaines plantes en produisent:
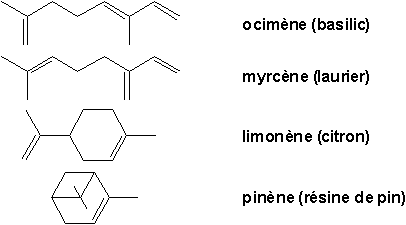
| Notions importantes 1 à 4 aux pages 403 et 404 Encarts des chapitres 11 et 12 Les problèmes 1 à 4, 6, 22, 25 des pages 404 à 412 peuvent être faits. |
7.2. Diènes, allènes, diènes conjugués et polyènes (Vollhardt 12.13, 14.5, 14.7 et Arnaud 20.1 à 20.6)
Un diène est une molécule qui possède 2 doubles liaisons carbone-carbone.
Les deux liaisons dun diène peuvent se trouver dans les positions relatives suivantes:
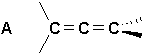
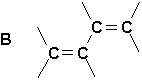
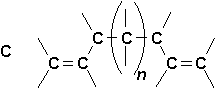
La structure A est celle des allènes, dont le premier terme est le propadiène (ou allène) (H2C=C=CH2). Ce sont des composés instables qui se transforment facilement en alcynes.
De plus, les allènes possèdent une particularité structurale intéressante. Les deux liaisons
p sont à angle droits lune de lautre, parce que latome de carbone central est hybridé en sp. Les orbitales 2py qui forment la liaison p avec un des atomes de carbone sont perpendiculaires avec les orbitales 2pz qui forment la liaison avec le second atome de carbone (Figure 14.5, Vollhardt p.510). En conséquence, les allènes substitués du type abC=C=Cba peuvent être chiraux, même sils ne possèdent pas de carbones asymétriques. Le 1,3-dichloropropa-1,2-diène en est un exemple: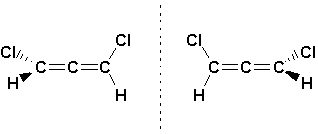
Si les doubles liaisons sont contiguës, il sagit dun cumulène
=C=C=C=C=C=C=C=C=C=
Dans la structure C, les doubles liaisons sont séparées par plusieurs liaisons simples et cela ninfluence en rien la réactivité des alcènes. Tout comme si ces molécules ne contenaient quune seule double liaison.
Dans la structure B, par contre, où les deux doubles liaisons sont conjuguées, leurs propriétés sont profondément modifiées par leur proximité. Elles réagissent comme un ensemble, constituant en quelque sorte un nouveau groupe fonctionnel, et leur spectre ultraviolet est fortement modifié. Le maximum dabsorption se déplace vers le visible (indiquant une plus faible énergie de transition à lintérieur de la molécule) et le coefficient dabsorptivité molaire,
e, augmente de façon drastique. Par exemple:Éthylène, H2C=CH2
Buta-1,3-diène, H2C=CHCH=CH2 lmax = 217 nm e = 21 000
b-Carotène, 11 doubles liens conjugués lmax = 496 nm e = 162 000
À partir de 5 doubles liaisons conjuguées, labsorption se produit dans la région violette du spectre visible, et en conséquence la substance apparaît colorée en jaune. À mesure que le déplacement saccentue vers le bleu, puis vers le vert du spectre, la couleur "sapprofondit" en passant à lorangé et au rouge.
Les polyènes conjugués qui possèdent la structure suivante:
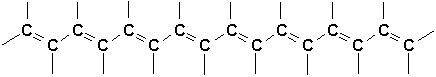
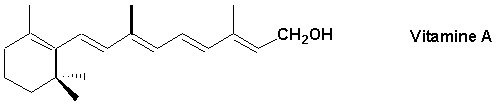
sont les plus intéressants; certains possèdent plus de dix doubles liaisons conjuguées et proviennent de substances biologiquement importantes comme le
b-carotène (le colorant orange des carottes) et la vitamine A (qui constitue son produit de métabolisation et dont laldéhyde est directement implique dans le processus de la vision.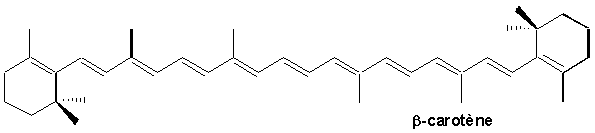
7.3. Ordre de liaison
p (Allinger 7.16)Les diènes conjugués sont stabilisés par résonance. Lordre de liaison
p est une mesure du caractère de double liaison entre 2 atomes. Une liaison simple possède un ordre de zéro (0). Une liaison double possède un ordre de un (1). On utilise la méthode LCAO (Linear Combination of Atomic Orbitals) pour évaluer la contribution des différents hybrides de résonance.Prenons le buta-1,3-diène. Les calculs LCAO montrent que ce lon croyait être:
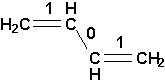
est en fait:
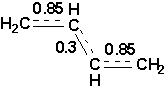
On utilise souvent la mesure des longueurs de liaisons pour mettre en évidence la stabilisation par conjugaison.
Ainsi, on peut prévoir pour le buta-1,3-diène que les liens C1-C2 et C3-C4 seront un peu plus grands quun lien double ordinaire, et que le lien C2-C3 sera un peu plus court quun simple lien ordinaire.
Expérimentalement, on ne peut mesurer de différences pour les liens doubles. Par contre, le lien C2-C3 mesure 1.47 Å. En se référant aux tables, on note quun lien Csp-Csp2 mesure 1.486 Å. La différence est due à la résonance.
Cette stabilisation est très importante et expliquera plusieurs propriétés des réactions des diènes conjugués.
7.4. Termes importants et utilisations (Arnaud 9-5)
Les alcènes industriellement les plus importants sont les premiers termes, éthène (éthylène) surtout, propène, butènes et méthylpropènes (isobutènes). Ils sont principalement utilisés dans la fabrication des polymères.
Certains diènes comme le buta-1,3-diène et le 2-méthylbuta-1,3-diène (isoprène) sont au départ de la fabrication des élastomères, ou caoutchoucs synthétiques.
Ces alcènes sont eux-mêmes obtenus des alcanes que lon trouvent dans le pétrole par des réactions (industrielles) de déshydrogénation à haute température.
La double liaison éthylénique est surtout importante pour les rôles variés quelle joue dans les mécanismes des organismes vivants:
Composés terpéniques, comme le rétinal (5 liens C=C) qui est responsable de la vision.
Squalène (C30H50) (6 liens C=C) point de départ de la synthèse du cholestérol
Phéromones (pherein, grec, porter; hormon, grec, stimuler) des insectes
| Encarts des chapitres 11 et 12 Les problèmes 17 et 19 des pages 456 à 465 peuvent être faits. |
7.5. Les alcynes (Vollhardt chapitre 13)
Les alcynes portent une triple liaison carbone-carbone et possèdent la formule générale: CnH2n-2. On les appelle souvent des hydrocarbures acétyléniques, du nom du premier terme de la série, lacétylène, HCº CH.
On distingue les alcynes monosubstitués, ou alcynes vrais: RC
+CH, et les alcynes disubstitués: RCº CR7.5.1. Nomenclature (Vollhardt 13.1)
La nomenclature des alcynes seffectue en changeant la dessinence -ane en -yne. De plus, à partir de C4, un indice de position est requis pour caractériser la position de la triple liaison. On utilise lindice de position le plus petit des deux carbones impliqués dans la triple liaison. Cette nomenclature est donc similaire à celle des alcènes.
7.5.2. Structure (Vollhardt 13.2 et 13.4)
Comme on peut le voir à la Figure 13.1 (Vollhardt p.468), la liaison triple provient dune liaison
s entre 2 orbitales sp et 2 liaisons p entre 4 orbitales 2p.La molécule est colinéaire, et ne possède donc pas disomères cis-trans. La longueur de la liaison carbone-carbone est plus courte que dans une liaison double. Il en va de même pour la liaison C-H, à cause du degré de caractère s élevé des orbitales hybrides. Cette liaison est également plus solide quune liaison double.
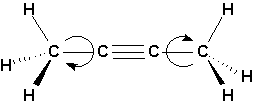
Le plus petit cycloalcyne non substitué isolé est le cyclooctyne. Cependant, il possède une tension très élevée, juste un peu plus faible que celle du cyclobutane. Le cyclohexyne et le cycloheptyne ont été signalés comme intermédiaires réactionnels instables: ce sont des alcynes courbes.
7.5.3. Caractères Physiques (Vollhardt 13.2 et Arnaud 10-1)
Léthyne (acétylène) (Point de Sublimation760 mm Hg -83°C), le propyne et le but-1-yne sont gazeux à la température ordinaire. Les autres termes sont liquide ou solide selon leur poids moléculaire.
Parce que les alcynes sont plus petits, plus effilés et plus compacts, les molécules peuvent sassocier de plus près, et donc augmenter les interactions de van der Waals. Conséquemment, les points de fusion et débullition de même que les densités sont légèrement supérieurs aux alcanes et alcènes de même nombre de carbone.
Les alcynes sont peu polaires, insolubles dans leau, mais solubles dans les hydrocarbures.
Les alcynes ont tendance à se polymériser facilement, et ce de manière violente (explosive dans le cas de lacétylène).
La formation de lacétylène à partir de carbone et dhydrogène (2 C + H2 ® C2H2) est fortement endothermique (D H=+230 kJmol-1), ce qui rend lacétylène instable. Il tend à se décomposer de façon violente lorsquil est comprimé ou liquéfié. Par contre il est très stable en solution dans lacétone en présence dune matière de remplissage poreuse comme la pierre ponce.
Tout comme les alcènes, les alcynes démontrent un moment dipolaire, sauf sils sont symétriques.
Finalement, certains hydrocarbures complexes du type suivant sont rencontrés dans le vide interstellaire et certaines huiles essentielles.
![]()
7.5.4. Réactivité (Arnaud 10-3)
Tout comme les doubles liaisons, les réactions que subissent les liaisons triples sont surtout des réactions daddition, parce que cette liaison triple est un site de forte densité électronique dont les électrons sont facilement accessibles car à cet endroit la molécule est linéaire. Les alcynes sont donc susceptibles aux attaques des réactifs électrophiles. Cest donc un maillon faible dans une chaîne hydrocarbonée et la molécule peut se briser plus aisément à cet endroit.
7.5.5. Liaison triple et RMN (Vollhardt 13.3)
Parce que le nuage électronique qui entoure la triple liaison est de forme cylindrique, la molécule sorientera dans le champ magnétique de façon à ce que leur mouvement crée un champ local qui soppose au champ externe dans le voisinage de lhydrogène alcynique (Figure 13.4, Vollhardt p.471). Il en résulte un effet de blindage qui contredit ce à quoi on sattendrait selon le comportement des alcènes. Il faut se rappeler que les carbones hybridés en sp sont plus électronégatifs que les carbones hybridés en sp2 ou sp3.
Le groupe fonctionnel alcyne transmet si bien le couplage que lhydrogène terminal est scindé par les autres hydrogènes, même sils sont séparés de lui par 3 carbones (couplage à longue portée) (Figure 13.5, Vollhardt p.471.
En ce qui concerne le RMN-13C, les carbones alcyniques absorbent dans une zone étroite entre 65 et 85 ppm, très différente de celle des alcanes et alcènes.
7.5.6. Termes importants et utilisations (Arnaud 10-4)
Le seul alcyne préparé couramment à léchelle industrielle est lacétylène. Toutefois, sa préparation est énergétiquement très coûteuse.
Avec les développements de la pétrochimie, les fabrications antérieurement basées sur lacétylène seffectuent maintenant avec léthylène. On ne sen sert plus quen laboratoire pour des synthèses de chimie fine et en soudure à très haute température.
La combustion de lacétylène dégage une chaleur importante parce que la chaleur de formation des produits sajoute à celle de la dissociation de lacétylène:
2 HCº CH + 5 O
2 ® 10 CO2 + 2 H2OD H= -1325 kJmol-1
Ainsi, la flamme de lacétylène atteint 2000°C dans lair et 3000°C dans loxygène.
Sa puissance calorifique est utilisé dans le chalumeau oxy-acétylénique qui brûle même sous leau! En outre, les particules de carbone incandescentes formées sont très éclairantes. Cest pourquoi ce gaz est utilisé dans les lampes à acétylène portées par les mineurs et les spéléologues.7.6. Degré dinsaturation (Vollhardt 11.6, Allinger 7.22)
Il est intéressant de noter ici le concept de sites dinsaturation. Ce concept indique le nombre de cycles/doubles liaisons dune molécule (en considérant quune liaison triple vaut deux liaisons doubles). Le nombre de sites dinsaturation nous donne le nombre de H2 nécessaire pour transformer le composé en produit saturé contenant le même nombre de carbones.
Le terme site dinsaturation est fréquemment utilisé, mais il ne reflète pas toujours la réalité. Ainsi, les cycloalcanes possèdent un site dinsaturation selon cette définition.
Comment calcule-t-on le nombre de sites dinsaturations lorsquil y a dautres atomes que le carbone et lhydrogène? Comme suit:
O
et S on les enlève car ils ne prennent la place de rienF, Cl, Br, I on les remplace par autant dhydrogènes
N et P on les enlève et on retire 1H en plus (donc on retire NH ou PH)
Exemple: C
7H12NO2SCldevient dabord: C7H12NCl (O
et S)
devient ensuite: C7H13N (halogènes)
devient enfin: C7H12 (NH et PH)
Un alcane de formule CnH2n+2 devrait être C7H16
Il manque donc 4H, ou 2H2,
ce qui indique 2 sites dinsaturations
La molécule possède donc 2 cycles, 2 liens doubles, un cycle et un
lien double, ou un lien triple.
On peut aussi appliquer les deux formules suivantes:
Hsat = 2 nC + 2 - nX + nN + nP
DI = ( Hsat - Hréel ) / 2
Exemple: C7H12NO2SCl:
Hsat = 2 nC + 2 - nX + nN + nP = (2x7)+2-1+1+0=16
DI = ( Hsat - Hréel ) / 2 = ( 16 - 12 ) / 2= 2
| Encart 13.1 et Sections 13.11 et 13.12 Notions importantes 1 à 5 aux pages 493-4 Les problèmes 1 à 3, 5, 6 des pages 494 à 500 peuvent être faits.
|
7.7 Exercices de nomenclature
Faire les exercices de nomenclature qui sont présentés dans Favre
Autres exemples: (réponses après les structures)
a) 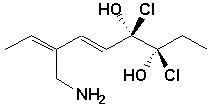 |
b) 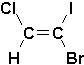 |
c)  |
d) 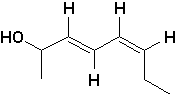 |
e)  |
f) 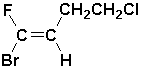 |
g) 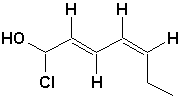 |
h) 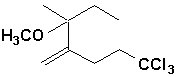 |
Réponses:
a) (3R,4R,5E,7Z)-7-aminométhyl-3,4-dichloronona-5,7-diène-3,4-diol
b) (Z)-1-bromo-2-chloro-1-iodoéthène
c) (3S,6E)-undéc-6-ène-1,10-diyn-3-ol
d) (3E, 5Z)-octa-3,5-dién-2-ol
e) (3S,4E,6E,8E)-déca-4,6,8-trién-1-yn-3-ol
f) (E)-1-bromo-4-chloro-1-fluorobut-1-ène
g) (2E, 4Z)-1-chlorohepta-2,4-dién-1-ol
h) 5,5,5-trichloro-2-(1-méthoxy-1-méthylpropyl)pent-1-ène
| Retour au menu |
|
ABCSITE © copyright 2000 |