abcsite.free.fr
![]()
Chimie Organique
|
|
10. Quelques produits dimportance biologique et industrielle
| Dans ce chapitre | |
| 10.1. | Glucides |
| Modèles Moléculaires en format .pdb: Cellulose et hémicelluloses | |
| 10.2. | Acides aminés et protéines |
| 10.3. | Lipides terpènes et stéroïdes |
| 10.4. | Chimie organique industrielle |
| Modèles Moléculaires en format .pdb: Produits Naturels | |
| Modèles Moléculaires en format .pdb: Drogues Synthétiques | |
| Modèles Moléculaires en format .pdb: Autres exemples | |
Nous allons terminer létude des structures de la chimie organique en abordant les composés qui possèdent une grande importance biologique: les monomères et polymères naturels.
10.1. Glucides (Vollhardt chapitre 23, Arnaud chapitre 22)
Les glucides constituent une classe de produits naturels dont le formule brute peut souvent être mise sous la forme C
m(H2O)n, doù lappellation qui leur est également donnée dhydrates de carbone. Toutefois, cette appellation est trompeuse, et la formule brute ne convient pas toujours à la vérité. Cest pourquoi il est préférable de les appeler des glucides.Les glucides sont des dérivés polyhydroxylés comportant en outre une fonction aldéhyde ou cétone. On les retrouve chez les végétaux et ils représentent un des produits importants de la photosynthèse.
6 CO2 + 6 H2O ® D-(+)-glucose (C6H12O6) + 6 O2
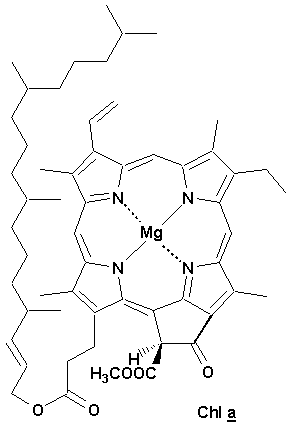
Cette étape seffectue chez les plantes vertes lorsquelles convertissent le bioxyde de carbone et leau en glucose et en oxygène sous laction de la lumière solaire. Le mécanisme détaillé de cette transformation est compliqué, et déborde le cadre de ce cours. Il suffit de dire que labsorption lumineuse dun quantum de lumière par la molécule de chlorophylle a incorporée dans un complexe protéique antenne est le premier stade de ce processus. Toutefois, le glucose nest pas le produit final de la photosynthèse: les plantes synthétisent à partir du glucose dautres glucides plus complexes comme lamidon, la cellulose et même des composés aromatiques, tels la lignine. De plus, il est important de noter que lacte primaire de la photosynthèse est dextraire des électrons de leau, de les transférer dans les centres réactionnels photosynthétiques et de là jusquau cycle de Calvin qui est lui responsable de la formation du glucose.
Dautre part, les acides nucléiques (ADN, ARN) porteurs des caractères génétiques héréditaires ont une structure partiellement glucidique.
Enfin, dans la vie pratique, la cellulose est liée à lindustrie du papier, des textiles naturels (coton) ou artificiels (rayonne, viscose), de la Cellophane, de matières plastiques (Celluloïd, Rhodoïd), dexplosifs, dadhésifs, ...
10.1.1. Oses et Osides
Les glucides sont divisés en deux grandes classes, les oses et les osides.
Les OSES sont des sucres simples, de 3 à 8 atomes de carbone. Ils possèdent tous des fonctions hydroxyles et soit une fonction aldéhyde dans le cas des aldoses, soit une fonction cétone dans le cas des cétoses.
Les osides sont obtenus par condensation des oses. Lorsque nous assistons à la condensation de plusieurs oses, nous obtenons des oligoholosides lorsque le nombre dunités est inférieur à 10 (saccharose, mannose, cellobiose), et des polyholosides lorsque le nombre dunités est supérieur à 10. On les appelle aussi des polysaccharides ou des osanes (cellulose, hémicelluloses, amidon, glycogène). Si la condensation seffectue entre un ose et une substance non glucidique, nous obtenons des hétérosides (coniférine, acides nucléiques).
10.1.2. Nomenclature (Vollhardt 23.1, Arnaud 21.1)
La nomenclature et les classes sont assez complexes, mais elles suivent la présentation ci-dessous:
Oses
: encore appelés monosaccharides ou sucres simples) Trioses, tétroses, pentoses, hexoses, ... (selon le nombre datomes de carbone)
Aldoses (contiennent la fonction aldéhyde)
Aldotrioses, aldotétroses, aldopentoses, aldohexoses, ...
Cétoses (contiennent la fonction cétone)
Cétotrioses, cétotétroses, cétopentoses, cétohexoses, ...
Osides
: résultent de la condensation, avec élimination deau, de molécules doses et, éventuellement, de substances non glucidiques également Holosides
: condensation doses uniquement Oligoholosides (ou oligosaccharides)
: moins de 10 unités doses Diholosides (disaccharides), triholosides (trisaccharides)
Polyholosides (ou polysaccharides ou osanes)
: nombre pouvant facilement aller jusquà 3000 et plus unités oses (cellulose, amidon) Hétérosides
: condensation doses et de substances non glucidique (appelées ici des aglycones) O-hétéroside
: aglycone lié à un ose par un atome doxygène N-hétéroside
: aglycone lié à un ose par un atome dazote10.1.3. Les Oses
Nous ne parlerons ici que des hexoses. Le glucose servira de modèle pour la série des aldohexoses, et le fructose pour les cétohexoses.
10.1.4. Aldohexoses: le glucose
Le plus important des trois aldohexoses est le (+)-(D)-glucose, principalement par suite de son abondance dans la nature et de la participation de la "structure glucose" à la constitution des oligo- et polyholoside les plus intéressants. Les deux autres aldohexoses existants à létat naturel sont le (+)-(D)-mannose et le (+)-(D)-galactose.
Décrivons rapidement les structures possibles du D(+)-glucose, un des 16 stéréoisomères (24) possibles (Figure 24.1, Vollhardt p.946, dernière rangée) pour une molécule ayant la structure suivante:
HOCH2C*HOHC*HOHC*HOHC*HOHC*HO
Il est important de noter que les formes D et L ont leur origine par rapport aux projection de Fisher des glycéraldéhydes.
À cause du nombre énorme de stéréoisomères possibles, il résulte que presque tous les aldoses et cétoses sont chiraux et possèdent une activité optique.
| Létudiant est invité à lire pour lui-même les sections 24.1 et 24.10 |
Le glucose peut exister sous une forme linéaire que lon appelle aldéhydique, où sous une forme cyclique que lon appelle hémiacétalique.
10.1.4.1. Forme ouverte (aldéhydique)
La structure du glucose naturel (+)-(D)-glucose est illustrée à la Figure du bas, Vollhardt p.947.
Cette structure particulière du glucose explique une bonne partie de ses propriétés chimiques, notamment la réactivité de la fonction alcool primaire.
10.1.4.2. Forme cyclique (hémiacétalique)
Toutefois, certains caractères des réactions de la fonction aldéhydique, par contre, ne sont pas toujours respectées. Divers arguments dordre chimique, à laide de synthèses de dérivés glucosidiques, conduisent à attribuer au glucose une tout autre image. Lexplication réside dans lexistence du glucose sous deux formes tautomères, dont lune est la forme aldéhydique ouverte, et lautre une forme cyclique dans laquelle la fonction aldéhyde nest pas libre, mais engagée dans un hémiacétal avec lhydroxyle du carbone 5 (Figure du bas, Vollhardt p.948).
Étant donné que lhétérocycle sapparente aussi au pyrane, on dorme à cette forme le nom de forme pyranose. Des formes cycliques se liant au carbone 4 ressembleront au furane, et porteront le nom de formes furanoses.
Léquilibre tautomère est très en faveur des formes cycliques (environ 95%), mais en présence dun réactif de la fonction aldéhyde le déplacement de léquilibre est assez rapide pour que le mélange se comporte en apparence comme sil nétait composé que de la forme ouverte.
Toutefois, cette cyclisation du glucose en forme hémiacétalique a pour effet de créer un nouveau carbone asymétrique, le carbone C1. Il y a donc deux stéréoisomères de cette forme cyclique, différant uniquement par la configuration de ce carbone. On les désigne par
a et b et on les appelle formes anomères (le carbone 1 est également appelé un carbone anomère) (Figure du haut, Vollhardt p.950).Pour ces deux formes cycliques, la représentation de Fisher est souvent abandonnée au profit de la représentation de Haworth (Figure du milieu, Vollhardt p.950).
Les anomères
a et b ne diffèrent que par la configuration du carbone 1. La forme la plus stable est la forme b, car alors tous les substituants hydroxyles sont en position équatoriale lorsque le cycle adopte la conformation chaise du cyclohexane (Figure du haut, Vollhardt p.951). La polymérisation des structures a mènera à la formation des amidons, alors que polymérisation des structures b mènera pour sa part à la formation de la cellulose.Lorsque lon met en solution lun ou lautre de ces deux anomères, on constate une évolution dans le temps du pouvoir rotatoire qui se stabilise après quelques heures. Ce phénomène, appelé mutarotation, résulte justement de lexistence de léquilibre tautomère entre les formes cyclique et ouverte, par suite duquel les deux anomères
a et b se trouvent en définitive en équilibre réciproque par lintermédiaire de la forme ouverte (Figure du milieu, Vollhardt p.952). Ainsi, les deux formes du glucose porteront-elles les noms de a-(D)-glucopyranose et b-(D)-glucopyranose.10.1.4.3. Cétoses: le fructose
La structure la plus fréquente pour les cétohexoses porte la fonction cétone sur le carbone 2 (Figure 24.2, Vollhardt p.946).
Comme le glucose, le fructose est fermentescible, i.e. quil peut fermenter, à la grande joie des fabricants de vins et dalcools.
10.1.5. Les Osides (Vollhardt 24.11 et 24.12, Arnaud 22-2)
Certains oses existent à létat libre dans la nature (glucose, fructose), mais beaucoup plus fréquemment aussi dans des structures glucidiques plus complexes.
Bien que le terme "glycoside" soit synonyme de "hétéroside", on emploie souvent lexpression liaison glycosidique pour désigner la jonction entre deux motifs dans un oside, quil sagisse dun holoside ou dun hétéroside (en dautres termes, que ces motifs soient tous deux glucidiques ou non).
10.1.6. Oligoholosides
Parmi les oligoholosides connus, 4 seulement méritent une attention plus marquée.
Le saccharose (Figure du haut, Vollhardt p.968), extrait de la canne à sucre ou de la betterave, constitue le sucre ordinaire et cest certainement le plus abondant et le moins cher des produits organiques purs préparés en grande quantité (production mondiale de 90 millions de tonnes par an). Il résulte de lassociation du D-glucose et du D-fructose.
(+)-saccharose + H2O ![]() (+)-(D)-glucose + ()-(D)-fructose
(+)-(D)-glucose + ()-(D)-fructose
Le maltose (Figure du bas, Vollhardt p.969), provient de lhydrolyse de lamidon. Il peut être hydrolysé à son tour et fournir deux molécules de
a-glucose:maltose + H2O ![]() 2
2
Le lien glycosidique est établi entre le carbone anomère de lun des cycles et le carbone 4 de lautre. Ce dernier cycle possède donc un carbone anomère libre (à lextrême droite sur la figure), de sorte quil peut exister une forme
La cellobiose (Figure du haut, Vollhardt p.970), produit de la dégradation de la cellulose, présente les même caractéristiques que le maltose. La seule différence entre ceux-ci réside dans la configuration du lien glycosidique sur le cycle lié par son carbone anomère: il est ici dans la configuration
b, alors quil était dans la configuration a dans le cas du maltosecellobiose + H2O ![]() 2
2
Le lactose (Figure du bas, Vollhardt p.970), se trouve à la teneur de 5% environ, dans le lait humain et de la plupart des mammifères. Son hydrolyse fournit une molécule de glucose et une molécule de galactose.
lactose + H2O ![]() glucose + galactose
glucose + galactose
10.1.7. Les Polyholosides
Les polyholosides (ou polysaccharides ou osanes) sont des substances de masse moléculaire très élevée, résultant de la condensation dun grand nombre doses. Les plus communs correspondent à la condensation dhexoses (particulièrement du glucose), et sont des hexosanes, mais il existe des composés analogues provenant de la condensation de pentoses (xylose par exemple), qui sont des pentosanes.
Les polyholosides les plus importants sont la cellulose, lamidon et le glycogène. Lenchaînement entre les cycles pyranose y est réalisé par une liaison glycosidique entre le carbone 1 (anomère) de lun et le carbone 4 ou le carbone 6 du suivant.
10.1.7.1. Cellulose
La cellulose est constituée par un enchaînement de cycles glucopyranose, avec une liaison glycosidique du type C1 (
b)-C4, de sorte que le motif principal, répété n fois, correspond à la structure du b-cellobiose (Figure du haut, Vollhardt p.971). La chaîne adopte la conformation linéaire car le lien que lon appelle disaccharide b-1,4 possède la particularité dorienter tous les liens hydroxyles du cycle en position équatoriale de la forme chaise que prend le cycle. Il en résulte ainsi une grande stabilité structurale.La valeur de n nest pas connue avec précision, car les méthodes utilisées pour déterminer la masse moléculaire provoquent souvent une dégradation partielle des chaînes. Toutefois, n est estimé entre 4 000 et 15 000 unités cellobiose par chaîne, ce qui donne un poids moléculaire variant entre 1,4 et 5 MD! Ceci est dû au lien glycosidique qui ici permet aux substituants du cycle pyranose de se retrouver tous en position axiale, permettant ainsi à la cellulose dadopter une forme linéaire.
La cellulose, qui constitue la paroi des cellules végétales, est un des principaux constituants du bois. Le coton est constitué de cellulose à 98%.
La cellulose est insoluble dans leau, mais son hydrolyse acide ou enzymatique donne du cellobiose.
Outre la fabrication du papier, les utilisations de la cellulose sont nombreuses:
Lestérification des fonctions alcools par HNO3 donne du nitrate de cellulose (improprement appelé nitrocellulose) utilisé dans la fabrication dexplosifs.
Le traitement à lanhydride acétique donne un acétate à partir duquel on obtient le Rhodoïd et la rayonne acétate.
La dégradation à laide du CS2 puis la régénération de cette cellulose modifiée mène au Cellophane et à la rayonne viscose.
La cellulose nest pas assimilable par lhomme, mais les ruminants peuvent lutiliser, après hydrolyse enzymatique au cours de la digestion, à la synthèse de leurs propres glucides.
10.1.7.2. Les hémicelluloses
Il existe une grande variété dhémicelluloses dont les chaînes sont constituées de sucre (oses) divers tels que les pentoses (xylose, arabinose) quon trouve en grande quantité dans les feuillus, les hexoses (glucose, mannose, galactose) particulièrement dans les résineux, ainsi que des acides uroniques. Ces chaînes peuvent être linéaires ou ramifiées selon le cas.
De plus, les hexoses qui les composent possèdent une structure moins stable que le glucose en position chaise. La stabilité des pentoses est encore moins bonne, ce qui explique la plus grande fragilité chimique démontrée par les hémicelluloses.
Ce sont des polymères ramifiés dont les degrés de polymérisation sont de lordre de quelques centaines. Les hémicelluloses sont liées à la lignine et à la cellulose.
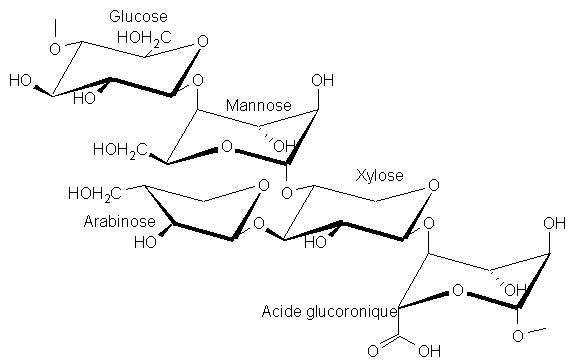
La figure suivante montre un exemple dhémicellulose:
10.1.7.3. Amidon
Dans le cas ou nous utilisons les formes
a-glucose (le disaccharide étant le maltose), nous fabriquons une structure spirale et non plus linéaire. Il en résulte une intégrité structurale moindre. Lamidon ne présente quune répétition de lordre de 200 unités de maltose (lien disaccharide a-1,4) dans sa structure et donc un poids moléculaire de lordre de 66 kD. De plus, lamidon est soluble dans leau.Lamidon est stocké notamment dans les graines et les racines des plantes, et constitue une réserve, source potentielle de glucose.
En général, lamidon est formé de deux constituants: lamylose (» 20%) (Figure du haut, Vollhardt p.972) et lamylopectine (» 80%) (Figure du bas, Vollhardt p.972)
Lamylopectine donne également du maltose par hydrolyse. La constitution des chaînes est donc similaire à celle de lamylose, mais la structure densemble est beaucoup plus complexe: plusieurs centaines de chaînes, comportant chacune 20 à 25 unités glucose, sont réunies selon un schéma ramifié, par des liaisons glucosidiques du type C1-C6, à une chaîne principale hélicoïdale.
10.1.7.4. Glycogène
Le glycogène, que lon retrouve dans le foie et les muscles des animaux présente des liens disaccharide
a-1,4 et disaccharide 4,6 et ainsi des chaînes courtes et un poids moléculaire de lordre de 15 MD.Le glycogène, analogue à lamylopectine, est produit et stocké par les organismes animaux pour constituer une réserve énergétique. Il comporte des chaînes plus courtes que lamylopectine, mais son poids moléculaire est extrêmement élevé, jusquà 15 millions! (Figure p.974).
10.1.8. Les Hétérosides
Les hétérosides, ou glycosides, sont des condensation doses et de substances non glucidique (appelées ici des aglycones). La liaison met en jeu le carbone anomère du glucide, de sorte quil peut exister des
a-hétérosides et des b-hétérosides. Laglycone peut se lié au glucide par un atome doxygène (O-hétéroside), ou par un atome dazote (N-hétéroside).On retrouve les hétérosides en abondance dans le monde végétal. En voici deux exemples:
Lamygdaline (qui se retrouve dans les amandes amères, et dont la partie glucidique est le gentiobiose et laglycone est la cyanhydrine du benzaldéhyde)
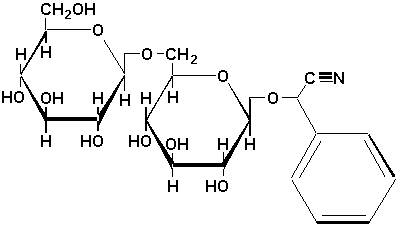
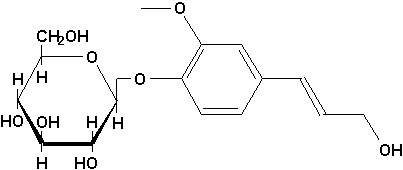
La coniférine (qui se retrouve dans la sève des conifères, et dont la partie glucidique est le glucose et laglycone est lalcool coniférylique)
| Encarts du chapitre 24 Notions importantes 1 à 6 et 11 à 1 3 p.981 Problèmes 1 à 8 p.981-987 |
10.2. Acides aminés et protéines (Vollhardt chapitre 26, Arnaud chapitre 23)
Le terme acide aminé, ou aminoacide désigne des composés où on retrouve à la fois une fonction amine et une fonction acide carboxylique. Outre que la fonction amine puisse être primaire, secondaire ou tertiaire, la position relative des deux fonctions peut varier:
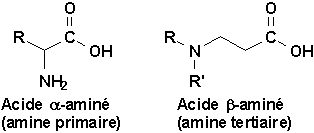
Parmi les acides aminés, ou aminoacides, sont particulièrement importants:
ceux dont le groupe amine est situé à lautre extrémité de la chaîne (
ceux dont les deux groupes fonctionnels sont contigus (
a-aminoacides) qui jouent un rôle essentiel dans la constitution de la matière vivante.10.2.1. Les acides
a-aminés (Vollhardt 26.1)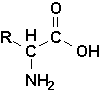
Le type le plus simple et le plus courant des acides
a-aminés dimportance biologique correspond à la formule générale de droite:Toutefois, certains, de structure plus complexe, comportent soit deux fonctions amines et une fonction acide (acides aminés basiques), soit deux fonctions acides et une fonction amine (acides aminés acides). Les acides aminés sont solubles dans leau, et leurs propriétés sont donc sensibles au pH (Tableau 26.1, Vollhardt p.1025-6).
Il est intéressant de noter que la plupart des aminoacides importants portent un nom particulier, par lequel ils sont toujours désignés.
10.2.2. Protéines et peptides (Vollhardt 26.4)
Les protéines sont les constituants essentiels de nombreux tissus vivants, végétaux ou animaux (protéines fibreuses formant la peau, les muscles, les cheveux, la soie, la laine), et en outre, jouent souvent un rôle primordial dans divers processus vitaux (enzymes, hormones, protéines globulaires comme lhémoglobine, lalbumine, déterminisme génétique, etc.) (Figures 26.2 à 26.5 p.1038-1040, Figures 26.7 à 26.9 p.1051-2).
Les protéines résultent de la condensation dun grand nombre de molécules dacides aminés selon le schéma de la figure du haut p.1035. Cette polycondensation conduit à des chaînes plus ou moins longues, linéaires ou cycliques. La liaison CONH qui constitue le groupement caractéristique de ces enchaînements est appelé liaison peptidique.
Les peptides ont une structure analogue, mais correspondent à la condensation dun nombre limité daminoacides, et il ny a pas de différences essentielle entre eux et les protéines, si ce nest la masse moléculaire. On fixe, de façon, arbitraire la limite entre les peptides et les protéines à une masse moléculaire de 10 000, celui des protéines pouvant atteindre plusieurs dizaines de millions.
Les protéines nont pas de point de fusion défini et subissent, sous laction de la chaleur, des transformations diverses irréversibles que lon nomme dénaturation. La coagulation du blanc duf à chaud en est un exemple.
Lorsquelles sont soluble, les protéines ne donnent pas des solutions vraies, mais des solutions colloïdales qui précipitent par addition dun électrolyte. La précipitation de la caséine en solution colloïdale dans le lait (doù sa couleur blanche) par laction de lacide acétique en est un exemple ("lait sûr" pour recettes de gâteaux).
Les enzymes sont des catalyseurs grâce auxquels saccomplissent dans les organismes vivants des réactions qui autrement seraient impossibles. Ce sont des protéines, mais certaines doivent leur activité à un groupe prosthétique, que lon nomme un coenzyme.
Les enzymes démontrent une action extrêmement spécifique en fonction des réactions à effectuer. Ainsi, une enzyme qui réussit à hydrolyser le maltose est totalement non efficace envers la cellobiose. Ceci explique pourquoi les ruminants digèrent la cellulose et que lhomme en est incapable. Ceci explique aussi pourquoi certains nourrissons sont incapables de digérer le lait de vache et doivent prendre des laits de soja parce quil leur manque lenzyme responsable de la dégradation du lactose.
Les toxines produites par des bactéries pathogènes ou contenues dans le venin de serpents sont aussi des protéines; mais elles exercent une activité catalytique ayant pour effet de bloquer laction denzymes nécessaires au métabolisme. Finalement, certaines enzymes, comme les phospholipases que lon retrouve dans le venin de crotale, ont pour effet de détruire certaines molécules, ici les lipides qui constituent les parois cellulaires provoquant la rupture de la paroi et la destruction des cellules.
10.2.3. Acides nucléiques (Vollhardt 26.9)
Les N-hétérosides dans lesquels la partie glucidique correspond au (D)-ribose ou au désoxy-2-(D)-ribose, et laglycone à diverses bases hétérocycliques du groupe de la pyrimidine et de la purine sont appelés ribonucléosides ou désoxyribonucléosides
Les acides ribonucléiques (ARN) et désoxyribonucléiques (ADN) présents dans le noyau des cellules vivantes ont formés de la réunion dun très grand nombre (3 000 à 10 millions) de tels hétérosides. La liaison entre les cycles est assurée par de lacide phosphorique qui estérifie les fonctions des carbones 3 et 5. On appelle nucléotide chaque motif complet comportant un groupe phosphate, un cycle glucidique et une base azotés. La masse moléculaire de telles chaînes peut varier de 1 million à 4 milliards, et ces molécules sont suffisamment grosses pour être vues au microscope électronique!
Les différentes bases et les différents nucléotides présent dans lADN sont présentés aux pages 1053 et 1054 dans Vollhardt. Le pairage entre les bases est montré à la Figure 26.11 (Vollhardt p.1055).
La structure de la molécule dADN [Note] est présentée à la Figure 26.12 (Vollhardt p.1055). La molécule senroule sous la forme dune double hélice à cause des liaisons hydrogène existant entre les différentes paires de bases complémentaires adénine-thymine et guanine-cytosine.
| Notions importantes 1 à 5, 8 et 9 aux pages 1061 et 1062 |
10.3. Lipides, terpènes et stéroïdes (Vollhardt 20.4 et 4.7, Arnaud 24)
Les termes lipides, terpènes et stéroïdes désignent des classes de composés naturels abondamment présents dans les règnes animal et végétal. Ils présentent certaines analogies du point de vue de leur biogenèse et jouent divers rôles importants dans de nombreux processus biologiques.
La diversité de ces séries, de même que leur complexité est effarante, et nous nen effleurerons ici que la surface.
10.3.1. Les agents tensioactifs: Cires, graisses, huiles, savons et détergents (Allinger 8.11, Vollhardt 20.4, Arnaud 24-1)
Les graisses et huiles naturelles, ainsi que les cires, sont principalement des mélanges complexes desters de poids moléculaire élevés. Ces composés sont connus sous lappellation globale de lipides.
Les lipides constituent une classe très hétérogène. Il ny a que peu de rapports entre un triglycéride (un corps gras) et une sphingomyéline (constituant du tissu nerveux), si ce nest la présence à peu près générale dans toutes ces molécules dacides gras.
10.3.1.1. Cérides
Les cires (cérides) sont des mélanges desters dacides gras et de monoalcools, comportant les uns comme les autres de 16 à 36 atomes de carbone, et de quelques alcanes à longues chaînes. Les acides portent parfois aussi des groupes hydroxyles.
Les cires de cachalot et dabeilles sont des exemple de cire dorigine animale (haut p.779):
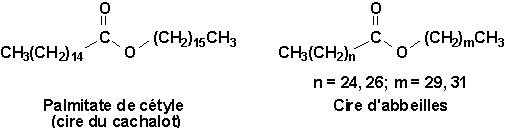
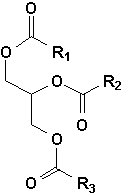
Les corps gras, graisses ou huiles, dorigine animale ou végétale (huile de lin, dolive, darachide, beurre, etc.) sont des triesters du glycérol et dacides gras portant couramment entre 12 et 22 carbones (Il est à noter que les graisses et huiles utilisées comme lubrifiants, les huiles minérales, sont essentiellement de mélanges dhydrocarbures). Ces esters sont fréquemment appelés glycérides (figure droite p.779).
Lorsque lon hydrolyse ces corps gras, on obtient le glycérol et les acides gras à létat libre. Par contre lors dune saponification (OH
), ces acides gras sont transformés en sels de sodium ou de potassium qui constituent les savons.10.3.1.2. Lipides complexes
Il sagit de composés complexes parfois très différents des glycérides, présents dans de nombreux tissus vivants dont voici deux exemples: les phosphatides et les lipoprotéines.
10.3.1.3. Les phosphatides (phospholipides)
Dérivés du glycérol, ils possèdent la structure générale suivante (Figure du bas p.779):
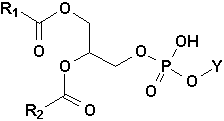
Ici, Y représente un groupement prosthétique quelconque, mais plusieurs proviennent de dérivés dacides aminés.
Un exemple est la phosphatidylcholine (lécithine) que lon retrouve abondamment dans le cerveau (Figure du bas p.779):
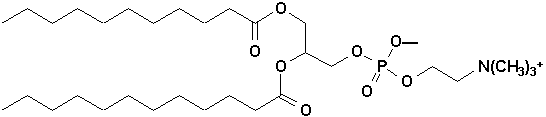
10.3.1.4. Rôle biologique
Les lipides constituent, avec les glucides et les protides lune des trois grandes classes daliments et, parmi eux, les triglycérides sont les plus courants (lait, huiles). Leur dégradation enzymatique dans lorganisme fournit la matière première à la biosynthèse de nombreux autres composés.
Dautre part, les lipides représentent pour lorganisme une forme de stockage de lénergie. Les calories alimentaires en excès sont utilisées à la synthèse des graisses. La combustion des lipides (38 kJ g-1) est plus énergétique que celle des glucides (17 kJ g-1).
Enfin, les lipides sont responsable du maintient de lintégrité de la paroi cellulaire.
10.3.1.5. Savons et détergents
Les savons sont des sels alcalins (de sodium ou de potassium) dacides acycliques à longue chaîne (16 à 18 carbones) comme le stéarate de sodium, CH3(CH2)16COOH. Leurs propriétés détergentes résultent dune balance des forces hydrophobes à lintérieur de la molécule.
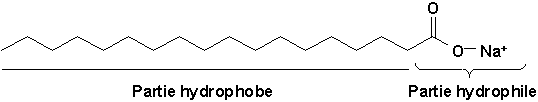
Ces molécules auront la particularité de sorienter à linterface air-eau de façon à ce que la tête polaire "trempe dans leau", et que la chaîne hydrophobe soit "dans lair". Sans entrer dans aucun détail, ce qui serait trop long ici et nous éloignerait ne notre sujet, il suffit de dire que toute la qualité et la subtilité de la fabrication des savons et détergents actuels réside dans la position déquilibre de cette balance hydrophile-hydrophobe (figures de la p.780).
Les détergents possèdent aussi des chaînes dacides gras, mais la partie polaire de la molécule, celle qui produit la solubilité dans leau, nest pas une fonction acide carboxylique. Ainsi, elle nest pas sujette à donner des précipité lorsque mis en présence dions de métaux lourds et alcalino-terreux comme Ca2+. Ils possèdent donc une plus grande plage dutilisation, et la plupart des détergents industriels possèdent des structures gardées secrètes.
Par contre on peut dire que plusieurs dentre eux ont des groupements sulfonates tel:
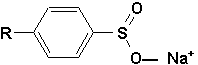
| Notion importante 5 à la page 814. |
10.3.2. Les terpènes (Vollhardt 4.7, Arnaud 24-2)
On retrouve ces composés très odoriférants dans végétaux doù on les extrait depuis longtemps sous la forme dhuiles essentielles (térébenthine, camphre, menthol, citronnelle) (Structures, Vollhardt p.125).
De nombreux composé terpéniques sont utilisés en parfumerie et certains dentre eux jouent des rôles biologiques importants (hormones, vitamines).
Au sens strict, les terpènes sont des hydrocarbures, mais certains composés possédant des fonctions oxygénées et une structure similaire sont également considérés comme des composés terpéniques.
Les formules brutes des hydrocarbures terpéniques sont:
| Monoterpènes | C10H16 |
| Sesquiterpènes | C15H24 |
| Diterpènes | C20H32 |
| Triterpènes | C30H48 |
| Tétraterpènes | C40H64 |
Certains ont une structure acyclique, dautres comportent un ou plusieurs cycles et une ou plusieurs doubles liaisons.
Les composés terpéniques oxygénés sont parfois moins insaturés que les hydrocarbures terpéniques correspondants (exemple le menthol et le limonène).
10.3.2.1. Règle isoprénique
Tous les composés terpéniques se présentent structurellement comme des polymères de lisoprène (C5H8), mais seulement en structure car la nature ne se sert pas de lisoprène pour biosynthétiser les terpènes.
En examinant avec détails les structures des terpènes, on peut retrouver ce motif à plusieurs reprises.
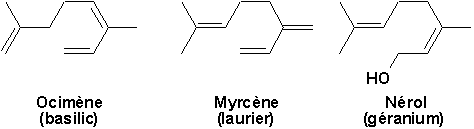
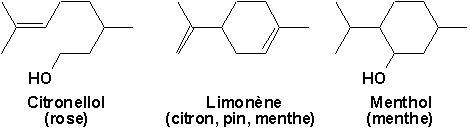
10.3.2.2. Monoterpènes
On les rencontre comme constituants odorants des essences végétales.
La plupart de ces composés possèdent des centres asymétriques et sont donc optiquement actifs. Dans la nature, on ne retrouve fréquemment quun seul des stéréoisomères.
L
a-pinène (ou térébenthine) constitue 20% de la résine du pin. Il est utilisé comme solvant et pour synthétiser le camphre.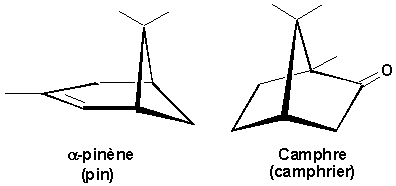
10.3.2.3. Diterpènes
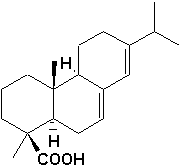
Lacide abiétique (ou colophane) est le constituant principal (80%) de la résine de pin. On lutilise entre autres pour lencollage du papier, ainsi que pour la préparation de vernis et de savons.
La vitamine A
est nécessaire à la croissance et à la vision. Cest un alcool primaire qui provient de la coupure oxydante du carotène (cest pourquoi on dit que manger des carottes cest bon pour la vue)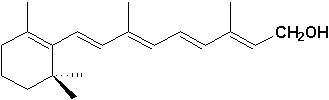
10.3.2.4. Tri- Tétra- et polyterpènes
Le squalène, extrait du foie de requin, est un triterpène important, précurseur du cholestérol. On peut écrire la chaîne linéaire C30H48, mais il est plus "suggestif" de le représenter de la manière suivante, qui fait apparaître une analogie effective avec la structure des stéroïdes:
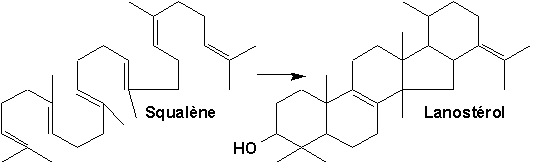
Le lanostérol, formé à partir du squalène par une série de cyclisation et de réarrangements, se transforme ultérieurement en cholestérol. Cest dautre part un constituant de la graisse de la laine (doù son nom).
Parmi les tétraterpènes les plus importants, citons le carotène dont nous avons déjà parlé qui donne la couleur orange aux carottes et aux feuilles dautomne.
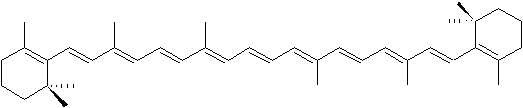
Un autre tétraterpène entièrement acyclique, le lycopène, se trouve notamment dans la tomate.
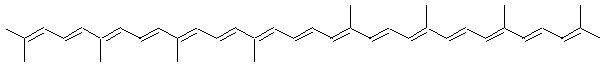
10.3.3. Les stéroïdes (Vollhardt 4.7, Arnaud 24-3)
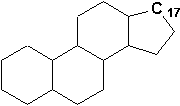
Les stéroïdes constituent une classe de composés abondamment présents dans la nature et contenant le squelette du perhydrocyclopentanophénanthrène (figure du haut, p.126) et portant en outre diverses fonctions ou insaturations, ainsi que des chaînes latérales sur le carbone 17.
Ce ne sont pas des terpènes mais ils présentent des liens avec les triterpènes du point de vue de leur biosynthèse.
10.3.3.1. Cholestérol
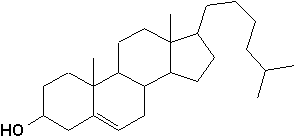
Cest le stéroïde le plus important. Isolé à la fin du xviii
e siècle à partir de calculs biliaires, sa formule exacte ne fut connue quen 1888 et sa structure complète quen 1955. Contenant 8 carbones asymétriques, il présente 28=256 stéréoisomères, dont un seul existe à létat naturel (voir aussi squelette général au haut de la p.126).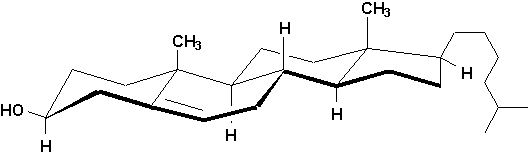
Le cholestérol est présent dans tous les tissus, soit à létat libre (calcul biliaires, tissu cérébral et tissu nerveux), soit sous forme desters (palmitate, stéarate, oléate).
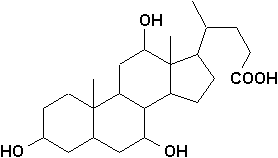
Il joue un rôle important dans la biogenèse des hormones stéroïdes et des acides biliaires comme lacide cholique (® à droite):
Ce dernier, sous forme de sels, facilite labsorption des graisses, en les émulsifiants comme le ferait un savon.
Une trop forte concentration de cholestérol dans le sang produit un dépôt dans les artères et leur durcissement (artériosclérose), doù le régime sans graisse imposé au personnes se trouvant aux prises avec ce problème.
10.3.3.2. Hormones sexuelles (Vollhardt 4.7, Arnaud 24.15)
Les caractères sexuels secondaires et la physiologie de la reproduction sont sous la dépendance dhormones mâles et femelles distinctes; leur structure est cependant peu différente, ce qui montre la finesse et la précision des mécanismes biochimiques.
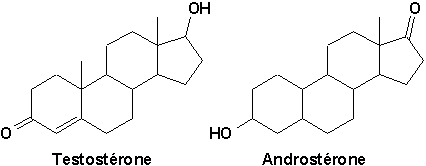
Les principales hormones mâles, sont la testostérone et landrostérone
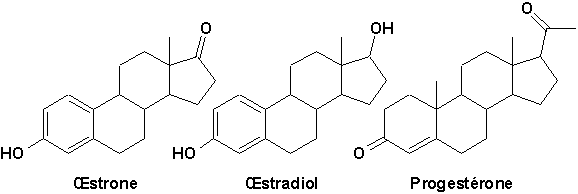
Trois hormones femelles sont particulièrement importantes: lstrone (ou folliculine) et lstradiol (ou dihydrofolliculine), qui règlent le cycle menstruel, et la progestérone, nécessaire à la grossesse:
10.3.3.3. Corticostéroïdes (Arnaud 24.16)
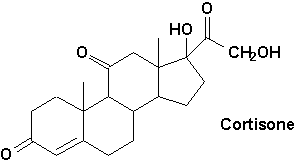
On nomme ainsi diverses hormones produites par les glandes surrénales, et dont la principale est la cortisone, utilisés dans le traitement de larthrite et des maladies inflammatoires.
| Encarts des chapitres 4 et 20 pas encore lus Notions importantes 13 à 16 aux pages 128-129 Problèmes 15 à 18, 21 des pages 129 à 135 |
10.4. Chimie organique industrielle (Arnaud chapitre 25)
La chimie organique nest pas seulement une science théorique et de laboratoire, cest aussi une science dont les applications concernent notre vie quotidienne. On la retrouve dans des domaines aussi différents que la santé, les loisirs, lhabillement et les transports. Cest la base dune industrie très diversifiée.
Par exemple, pour les chiffres de la fin des années 80 en France, sur un total de 317 milliards de francs pour la totalité de lindustrie chimique française, la part de la chimie organique atteignait 280 milliards, i.e. 88%. Pour la France, la seule industrie des parfums rapporte deux fois plus que lindustrie automobile.
10.4.1. Grandes sources de matières premières
Parmi les trois sources principales de matières premières pour lindustrie chimique organique: houille, pétrole et biomasse végétale, cette dernière a pour principal intérêt de fournir des composés déjà relativement complexes, et surtout de la cellulose, ainsi que dautres glucides dont la synthèse ne serait pas possible. Mais, les matières de base les plus fondamentales sont fournies par les deux premières.
10.4.1.1. La houille
La houille provient de la fossilisation des végétaux des temps préhistoriques, sous laction des bactéries dune part, de la température et de la pression du sous-sol dautre part.
De 10 à 40% de la masse de la houille est constituée de produits organiques plus ou moins volatiles, dont la nature et les proportions dépendent de lâge de la houille. La houille est un polymère amorphe constitué de couches de composés aromatiques et hydroaromatiques polycycliques faiblement liés entre eux (Figure 25.6, Vollhardt).
On distille la houille en absence dair à une température comprise entre 500°C et 1 100°C suivant les cas pour obtenir (par tonne de houille):
100 à 400 m3 de gaz (H2=50%, CH4=30%, CH2=CH2, CO, CO2, NH3)
7 à 10 kg de benzol, qui donne du benzène, du toluène et des xylènes par distillation
30 à 100 kg de goudron, dont la composition est fonction de la température atteinte. Cette fraction contient plus de 100 constituants différents
650 à 800 kg de coke formé de carbone et de composés minéraux
10.4.1.2. Le pétrole
Bien que son exploitation soit plus récente que celle de la houille, le pétrole constitue de nos jours la base principale de lindustrie chimique organique.
Les principales opérations de traitement du pétrole brut sont les suivantes:
Distillation. Elle permet de fractionner le pétrole en un certain nombre de coupes correspondant à lensemble des constituants dont les points débullition sont compris entre deux valeurs déterminées.
Craquage (Cracking). Les fractions obtenues par distillation ne correspondent généralement pas au besoins de lindustrie. En particulier, on dispose dune surabondance de fractions lourdes, et pas assez de fractions légères. Sous laction de la chaleur, souvent accompagné dun catalyseur, on cause des ruptures de chaînes pouvant ainsi augmenter la proportion des fractions légères.
Reformage (Reforming). Les moteurs modernes exigent des carburants de haute qualité et les essences obtenues lors des opérations précédentes ne correspondent pas toujours aux spécifications exigées. Le reformage a pour objet daméliorer leur qualité en provoquant, sous laction de la chaleur et de catalyseurs, des isomérisations des chaînes linéaires en chaînes ramifiées, ainsi que des cyclisations et des déshydrogénation conduisant à des cycles benzéniques.
Vapocraquage (Steam-cracking). Cette opération vise à produire des alcènes. Ce procédé consiste à soumettre pendant une fraction de seconde à 800°C des hydrocarbures léger vaporisés en présence de vapeur deau.
Lindustrie possède ainsi de vastes ressources et ses applications sont pour ainsi dire illimitées. Il suffit de nommer:
Éthylène
Textiles et explosifs, solvants et peintures, cosmétiques et détergents, colorants, insecticides, polymères
Propène
Solvants et peintures, textiles et cosmétiques, colorants, dérivés fluorés, résines et polymères
Benzène
Résines, solvants, détergents, colorants et explosifs, insecticides et pesticides, polymères
10.4.2. Hauts polymères
Les hauts polymères sont des macromolécules de très grande masse moléculaire.
Les principaux polymères daddition obtenus dans lindustrie en fonction des monomères de départ sont présentés ici:
Éthylène: Films, feuillages, câbles, moulages, bouteilles
Propène: Articles moulés (automobile, mobilier)
Chlorure de vinyle: Tuyaux, films, feuilles, câbles, chaussures
Styrène: Bacs, meubles, jouets. Expansé (98% air) = emballages anti-choc, isolants thermiques et phoniques
Tétrafluoroéthylène: Revêtements thermorésistants
Butadiènes: Pneumatiques, chambres à air, tuyaux, caoutchouc
| Encarts de tous les chapitres pas encore lus |
| Retour au menu |
|
ABCSITE © copyright 2000 |