|
Série
5 (suite):
Changement de phase d'un corps pur
|
Exercice
3:
Formule
de Clapeyron. Point triple de leau
On se propose détudier les équilibres entre les phases
solide, liquide et gazeuse de leau au voisinage du point triple
qui correspond à une température t0
= 0,01 °C.
1-
Donner léquation de lisotherme relative à 1
g deau pour la température de 0
°C, en admettant que la vapeur deau peut être assimilée à
un gaz parfait, et sachant que la pression de vapeur saturante de la
glace est, à 0 °C, de 4,60
mm de mercure. On exprimera les volumes en cm3
et les pressions en mm
de mercure.
2-
On admet que la courbe de sublimation et la courbe de fusion peuvent
être assimilées à des droites entre 0
°C et la température du point triple.
Sachant
que la chaleur de sublimation de la glace à 0
°C est égale à 684
cal/g, calculer la pression du point triple.
3-
Calculer la chaleur de fusion de la glace à la température de 0
°C.
On
donne :
uS =
1 cm3/g , uL
= 1,09 cm3/g et
Vmolaire (de la vapeur deau) : =
22,4 litres.
Solution
3 :
1-
Léquation
de lisotherme est p
v = cte. Le point
p =
4,6 mm Hg = 613,3 Pa ,
v
= vv =
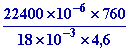 =
205,603 m3
=
205,603 m3
(car 760x0,022 = 1xRx273 et 4,6xV = (1/18)
xRx273 et
v = 205,603
m3)
appartient à
lisotherme, donc :
p
v = 126096 J
2-
La
chaleur de sublimation est donnée par la formule de Clapeyron ,
en
négligeant le volume massique du solide par rapport à celui de la vapeur, on obtient :
Ls = T vV
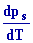 (
car
Ls = T(
vV
-
vS )
(
car
Ls = T(
vV
-
vS )
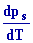 et vS
«
vV )
et vS
«
vV )
Doù
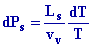
donc
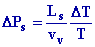 =
=
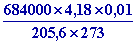 =
0,51
Pa =
0,004 mm Hg
=
0,51
Pa =
0,004 mm Hg
et la
pression du point triple :
PT
= 4,60
+ 0,004
= 4,604
mm Hg.
3-
La chaleur de fusion est donnée par la formule de
Clapeyron :
LF
=
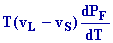
Avec
dPF = DPF
= 760 4,604 = 755,396 mm Hg
, dT =
DT=
0,01 °K.
Par suite,
LF
=
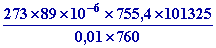 =
349570 J/kg
= 83,63 cal/g
=
349570 J/kg
= 83,63 cal/g
|