|
Série 5:
Changement de phase d'un corps pur
|
EXERCICE
1 :
On
considère 600 g deau
à la température t = 60 °C
quon mélange à 500 g
de glace à la température t2
= - 14 °C.
Si
la température déquilibre tf
est
supposée nulle, déterminer les masses finales respectives deau
et de glace?
On
donne : Ce
= 1
cal / g °K ,
Cg
= 0,5 cal / g °K ,
Lf
= 80 cal / g
Solution
1 :
A la température tf = 0 °C ,quand
il y a changement de phase :
¨
ou bien on a fusion
dune partie de la glace,
¨
ou bien on a solidification dune
partie du liquide.
Dans
les deux cas on écrit ; Qp
= x L
avec :
·
x > 0 si le
changement détat est une fusion.
·
x < 0 si le
changement détat est une solidification.
Conclusion :
 est la quantité de
glace ou de liquide qui sest transformée.
est la quantité de
glace ou de liquide qui sest transformée.
On écrit : ( en tenant compte que tf
= 0 °C )
DU
= 0
= Qeau +
Qglace + x L
= 0
doù meCe
( Tf -
T1 ) +
mgCg ( Tf - T2
) + x L
= 0
x = -
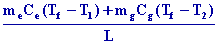
x
=
-
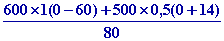 = 406,25 g
= 406,25 g
Comme
x > 0 , donc il y
a 406,25
g de glace qui sest transformée en eau ; on obtient :
·
600 + 406,25 g =
1006,25 g deau
·
500 406,25 =
93,75 g de glace
Exercice
2:
1-
a)1
litre
deau liquide est introduit dans une enceinte vide de 5
m3. La température est fixe et vaut 50
°C. En utilisant la formule de Duperray,
expliquer que se passe-t-il ?
b)En
admettant que la vapeur deau se comporte comme un gaz parfait,
combien y a-t-il deau
vaporisée à léquilibre ?
2-
Dans un récipient clos de 5
m3 contenant de lair sec à la pression 0,8
atm et à la température de 50
°C, on introduit 1
litre deau.
a)
Que
se passe-t-il en supposant que la température est maintenue
fixe?
b)
Quelles
sont à léquilibre les valeurs de la pression partielle de
lair, de leau vaporisée, et de la pression totale ?
quelle est la quantité deau vaporisée ?
Solution
1 :
1-
a
)
Pour calculer la pression de vapeur saturante de leau à t
= 50 °C, utilisons la formule de Duperray
PS = fS(T)
= P0
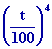 ( P0
= 1 atm et t en °C ) ;
( P0
= 1 atm et t en °C ) ;
On
trouve
PS =
0,062 atm = 6331
Pa.
Leau introduite dans lenceinte vide, va
se vaporiser jusquà ce que la pression de la vapeur atteigne la
valeur de la pression
de vapeur saturante.
b
) A
léquilibre, on suppose que leau vaporisée occupe tout le
volume de lenceinte, ( cest à dire 5
m3 ) et que cette vapeur deau ( à PS
= 6331 Pa )
se comporte comme un gaz parfait ;
le
nombre de moles vaporisées est alors n
=
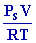 =
=
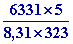 = 11,8 moles
= 11,8 moles
ce
qui correspond à m
= n M = 11,8 ´ 18 = 212 g deau.
2-
Dans un récipient clos de 5
m3, où la pression initiale dair
est 0,8
atm à 50 °C, leau
introduite va sévaporer jusquà ce que la pression partielle
de leau atteigne la pression de vapeur saturante ( calculée en 1-
a
).
A
léquilibre, la pression partielle de lair est 0,8 atm, la pression de leau vaporisée vaut 0,062 atm et la pression totale vaut 0,862 atm.
Pour
lévaporation seule compte la pression partielle de vapeur ( qui
est la même que précédemment ) : la quantité deau
vaporisée sera donc la même, soit 212
g.
|