|
Série 3: Le
second principe de la thermodynamique
|
EXERCICE 1:
Une personne respire 12 l dair par minute à la température de 20 °C et le rejette à 45 °C. En considérant que lair est un gaz parfait diatomique de masse molaire M = 29 g/mole ; calculer la quantité de chaleur fournie pour le réchauffement de lair respiré en 24 heures. On suppose que la composition de lair reste inchangée entre linspiration et lexpiration sous une pression constante dune atmosphère.
On donne : la masse volumique de lair
r
= 1,24 Kg.m-3 ;
la constante des gaz parfaits R = 8,32 S.I.
Solution 1:
La masse dair réchauffée en 24 h est :
m = r
V n24
avec r : masse volumique , V : volume dair,
n24 : nombre de minutes en 24 h
d'où m = 1,24x 12 10 3
x60x 24 = 21,427 kg
Le nombre de moles dair est : n = 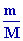 =
= 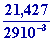 =
738,86 moles. =
738,86 moles.
La quantité de chaleur fournie pour le réchauffement de lair respiré en 24 h est :
Qp = n Cp DT
avec Cp = 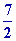 R gaz diatomique R gaz diatomique
Qp = 738,86
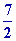 8,32 x ( 45 20 ) = 537,882 KJ
8,32 x ( 45 20 ) = 537,882 KJ  538 KJ 538 KJ
Remarque :on utilise Cp car la pression est supposée constante, alors que le volume varie au cours de la transformation.
EXERCICE
2:
a- Calculer la pression atmosphérique à laltitude z ; sachant que les conditions atmosphériques au sol sont caractérisées par la température
T0 et la pression P0 et que la température varie avec laltitude selon la loi : T =
T0 k z .
b- Déterminer la relation liant laltitude z à la pression P au cours de lascension dune masse dair (en le supposant comme gaz parfait) qui sélève dans latmosphère sans échange de chaleur avec lextérieur (dune façon adiabatique).
On donne : z = 4000 m ; P0 = 750 mm Hg ; T0 = 293 °K; g = 10 m
s-2
k = 0,005 °K /m ; r0
= 1,19 Kg.m-3 ; g
= CP
/Cv
= 1,4
Solution
2:
1- La différence de pression entre deux points daltitude z et z + dz est donnée par léquation de lhydrostatique : dP = -
r
g dz où la masse volumique r de lair ( gaz supposé parfait) est : r =
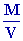 avec PV = RT , soit
r
= avec PV = RT , soit
r
= 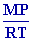
on en déduit dP = - P 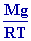 dz , soit dz , soit
 = - = -
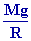 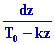
Intégrons entre laltitude O et laltitude z ; il vient : Ln 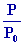 = = 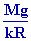 Ln Ln
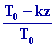
La relation pression - altitude sécrit donc : P(z) =
P0 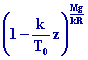
2-
Relation ( T, P )
Lorsque la masse dair passe de laltitude z à laltitude voisine z + dz, sa pression passe de P à P + dP et sa température de T à T + dT de façon à satisfaire la loi adiabatique
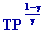 = cte que lon écrit sous la forme différentielle : = cte que lon écrit sous la forme différentielle :
 + +
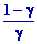  = 0
¬ = 0
¬
· Relation ( P, z )
Léquation fondamentale de lhydrostatique sécrit :
dP = - r
g dz avec PV = RT pour une mole dair,
donc : r
= 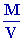 = =
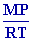 ,
soit dP = - ,
soit dP = -
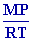 g dz ou g dz ou
 + +
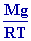 dz = 0
® dz = 0
®
· Relation ( T, z )
Éliminons la pression P entre ¬
et ®, il vient : dT +
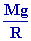 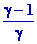 dz = 0 dz = 0
On en déduit le gradient vertical de température, correspondant à léquilibre adiabatique de latmosphère
Ka = 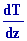 = - = -
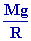 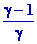 ¯ on pose
Ka = - ¯ on pose
Ka = -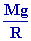 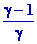 =cte =cte
A.N
Ka = - 9,76 10-3 k / m
Le gradient thermique Ka est constant, si on suppose g
et g constants,
on obtient donc en intégrant ¯ T =
Ka z + T0 ,
soit T = T0
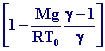 °
et P = P0 °
et P = P0 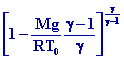 ±
car ±
car 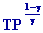 = cte = cte
La masse volumique de lair à laltitude z est daprès ,
°
et ± :
r =
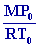
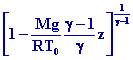
|