|
Chapitre
9:
THÉORIE
CINÉTIQUE DES GAZ PARFAITS
|
1- Définitions
:
a. Gaz parfait
Un gaz parfait est un système matériel d'un grand nombre de molécules identiques
- assimilables à des points matériels
- sans interaction mutuelle (l'énergie mécanique apparaît uniquement sous forme d'énergie cinétique)
- dont les directions des vitesses sont distribuées de façon isotrope.
b. Mole Volume molaire
* On appelle mole ou masse molaire M d'une substance la masse exprimée en grammes de N molécules de la substance
:
M = N m
N = 6,02 x 1023
(nombre d'Avogadro)
M est la masse d'une molécule.
* On appelle volume molaire
VM d'un gaz le volume occupé par les N molécules dans les conditions normales (pression : 1 atm., température : 0°C).
VM
= 22.4 litres
c. Vitesse quadratique moyenne
Le carré de la vitesse quadratique moyenne vq.m est égal à la moyenne
des carrés des vitesses de chaque molécule constituant le gaz.
Si N est le nombre total de molécules :
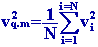
d. Énergie cinétique moyenne
* L'énergie cinétique moyenne est définie dans le référentiel du centre de masse
* L'énergie cinétique moyenne d'une molécule de masse m est donnée par :

* Dans le cas de N molécules
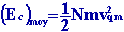
2- Pression d'un gaz
* Elle est la conséquence des collisions des molécules sur les parois de l'enceinte.
* La pression p d'un gaz qui s'exerce sur les parois d'un récipient a pour expression :

n : nombre de molécules par unité de volume
* La pression s'exprime en N.m-2 ou en atmosphère : 1 atm = 1,013
.105 N.m-2
3.Température d'un gaz
* La température est liée à l'état d'agitation des molécules du gaz.
* La température absolue T d'un gaz est proportionnelle à l'énergie cinétique moyenne d'une molécule.

k = 1,38 .10 - 23 J/K (constante de Boltzmann)
T = 273,15 + t°
(T est exprimé en degrés Kelvin et t en degrés Celsius).
4.Equation d'état d'un gaz parfait
La pression et le volume d'un gaz parfait, comprenant N molécules sont liés par la relation
:
p V = N k
T
5. Travail
Le travail d'un gaz dont le volume varie de V1 à V2 s'écrit :
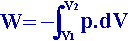
P : pression du gaz
Si W>0, le gaz " reçoit " du travail du milieu extérieur et si
W<0, le gaz
" fournit " du travail au milieu extérieur.
|