|
Chapitre
8:
POTENTIELS
THERMODYNAMIQUES
|
1.
ÉNERGIE LIBRE F ,
ENTHALPIE LIBRE
G
1.1.
Définitions
On
définit à partir des fonctions détat énergie interne U et
enthalpie H dun système et des variables conjuguées T et S, les
nouvelles fonctions détat suivantes :
Énergie
libre :
F = U - TS
Enthalpie
libre :
G = H - TS
1.2.
Différentielles
Pour
un système fermé fluide soumis uniquement aux forces de pression :
dF
= - SdT pdV
dG
= - SdT + Vdp
Pour
un système fermé pour lequel dW
=
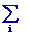 Yi dXi représente la somme des travaux, on généralise
les définitions de lénergie libre et de lenthalpie libre en
écrivant les différentielles sous la
forme :
Yi dXi représente la somme des travaux, on généralise
les définitions de lénergie libre et de lenthalpie libre en
écrivant les différentielles sous la
forme :
dF = - SdT +
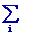 Yi dXi
Yi dXi
dG = - SdT
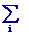 Xi
dYi
Xi
dYi
Pour
un fil élastique de longueur L soumis à une forme de traction Á :
dF = - SdT + Á
dL
dG = - SdT LdÁ
Pour
un diélectrique de permittivité relative er
(p, T) placé dans un condensateur de charge q sous la différence
de potentiel U :
dF = -
SdT pdV +
Udq
dG = - SdT + Vdp qdU
2.INTERPRETATION
PHYSIQUE
Lors
dune transformation monotherme dun système avec une source de
température T0 on peut écrire :
DF =
DU
T0 DS
= W + Q T0 DS
DG = DH
T0 DS
= W + Q + D(pV)
- T0 DS
DS = (Q/ T0)
+ Sp ³
Q/ T0
2.1 Pour lénergie libre
On
en déduit pour une telle transformation :
DF
£
W
La
variation dénergie libre est donc inférieure, ou dans le cas réversible
égale, au travail échangé.
Si
dans une transformation monotherme le système fournit du travail au
milieu extérieur, ce travail est au plus égal à la diminution
dénergie libre du système doù la dénomination de cette
fonction.
Si
de plus le système soumis uniquement aux forces de pression subit
une transformation isochore : DF
£
0
Les
transformations spontanées monothermes dun système soumis aux
seules forces de pression entraînent une diminution de F pour les
transformations isochores : DF
£
0
2.2 Pour lenthalpie libre
On
en déduit pour une telle transformation :
DG
£
W +
D
(pV)
Cette
relation prend une forme particulièrement simple si la
transformation est de plus monobare car W +
D
(pV) = 0 et on a donc : DG
£
0.
Les
transformations spontanées monothermes dun système soumis aux
seules forces de pression entraînent une diminution de G pour
les transformations monobares : DG
£
0.
Tout
système évoluant dans lune ou lautre de ces conditions
pourra aboutir à un état déquilibre où sa fonction F ou G
sera donc minimale.
Ces
fonctions qui jouent un rôle analogue à celui de lénergie
potentielle en mécanique sont pour cette raison appelées potentiels
thermodynamiques.
3.
PROPRIÉTÉS DES DIFFÉRENTIELLES
3.1 Relations de Maxwell
Pour
un système soumis aux seules forces de pression, en écrivant que
dU, dH, dF et dG sont des différentielles totales, on obtient en
particulier les relations suivantes :
S = -
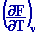
S = -
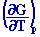
3.2 Relations de Gibbs-Helmholtz
En
éliminant lentropie S des expressions de F et G, on trouve :
U = F T
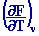
H = G T
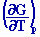
|