|
Chapitre
3:
COEFFICIENTS
THERMO ÉLASTIQUES ET CALORIMÉTRIQUES
|
1.
COEFFICIENTS THERMOELASTIQUES
1
1-1. Définitions
a
= 1 / V
 en K-1
en K-1
b
= 1/ P
 en
K-1
en
K-1
- isotherme : cT
= - 1/V
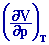 en
Pa-1
en
Pa-1
- isentropique : cS
= - 1/V
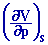 en
Pa -1
en
Pa -1
1.2 Relation entre coefficients thermo élastiques
cT
= =
g
cS
(relation de Reech) a
= pbcT
2.COEFFICIENTS CALORIMÉTRIQUES
On
étudie un fluide, système fermé monophasé, qui est défini par
sa pression p, son volume massique n
et sa température T. Ce système sera appelé système (p, n,
T). Ces variables sont reliées par une équation détat :
f (p, n,
T) = 0
Deux
variables seulement sont indépendantes : le système est divariant :
Cette
équation détat peut se présenter également sous les trois
formes :
p = p (n,
T) n
= n
(p, T) T = T (n,
p)
Pour
une transformation élémentaire quasi statique dun système (p, n,
T), la chaleur élémentaire par unité de masse dQ
sécrit en fonction de deux variables indépendantes :
δ Q = cn
dT + ldn
δ Q = cp dT + hdp
δ Q = l
dp + mdn
Ces
relations introduisent six coefficients calorimétriques.
La
variation élémentaire de lénergie interne relative à lunité
de masse sécrit :
du = cn
dT + (l p) dn.
La
variation élémentaire dh denthalpie relative à lunité de
masse sécrit :
dh = cp dT +
(h + n)
dp.
cn
= (T, n)
=
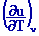
cp = (T, p) =
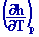
Cn,m
= M cn
et
cp,m =
M cp en J. mol 1
K -1.
Cn
= m cn
et Cp
= m cp
en J.K-1
On pose
g = Cp
/ Cv
3.
RÉSULTATS EXPÉRIMENTAUX
3.1 . Capacités calorifiques des solides
Les
solides subissent de faibles variations de volume ce qui permet de
parler généralement de la capacité calorifique c massique dun
solide :
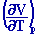 =
0 Þ
l =
0 Þ cp = cv =
c.
=
0 Þ
l =
0 Þ cp = cv =
c.
La
capacité calorifique dun solide augmente avec la température.
Au
dessus dune certaine température, la capacité calorifique
molaire Cm des solides reste pratiquement constante :
Cm = 3 R »
25 J.K -1 mol -1 (loi Dulong et Petit)
Avec
R la constante des gaz parfaits.
A
température ordinaire, cette loi est assez bien suivie par les
solides purs usuels.
3.2. Capacités calorifiques des liquides
Comme
les solides, les liquides subissent de faibles variations de volume
ce qui permet de parler généralement de la capacité calorifique c
massique dun liquide.
La
capacité calorifique dun liquide augmente avec la température.
La
capacité calorifique massique c de leau a la valeur la plus élevée :
c
= 4 187 J.K -1 kg-1 à température
ordinaire.
Les
liquides organiques comme léthanol ont une capacité calorifique
massique denviron 2 500 J.K 1 kg-1
à température ordinaire.
3.3 Capacités calorifiques des gaz
Pour
les gaz monoatomiques comme les gaz rares, on trouve à température
ordinaire des capacités calorifiques molaires telles que :
Cp, m = M cp
= 5/2 R = 20,8 J.K 1 mol -1
Cv,
m = M cv =
3/2 R = 12,5 J.K 1 mol -1
g
= 5/3 = 1,66
Pour
les gaz diatomiques comme le dihydrogène, le diazote, le dioxygène,
on trouve à température ordinaire des capacités calorifiques
molaires telles que :
Cp, m = M cp
= 7/2 R = 29,1 J.K 1 mol -1
Cv,
m = M cv =
5/2 R = 20,8 J.K 1 mol -1
g
= 7/5 = 1,4
|