|
Chapitre
2:
PREMIER PRINCIPE DE LA THERMODYNAMIQUE
|
1.
LE PREMIER PRINCIPE : CONSERVATION DE LÉNERGIE
1.1
Énergie interne U, énergie totale E
Pour tout système, il existe une fonction détat appelée énergie interne U, telle que lénergie totale E, fonction extensive, somme de lénergie cinétique macroscopique Ec, de lénergie potentielle extérieur Ep et de lénergie interne U soit conservative :
E = Ec + Ep + U
Ec est lénergie cinétique macroscopique due au mouvement densemble du système dans le repère détude.
Ep est lénergie potentielle provenant des forces extérieures : forces électromagnétiques, forces de
pesanteur.
Lénergie interne U sinterprète comme la somme de lénergie cinétique microscopique
Ec, micro des particules du système et de leur énergie potentielle dinteraction
Ep,int.
U =
Ec, micro + Ep,int.
1.2
Bilan
énergétique
La variation dénergie totale dun système fermé se réduit
à lénergie échangée à travers la surface avec le milieu extérieur
sous forme :
-
de travail W des forces extérieures appliquées en chaque
point de la surface ;
-
de chaleur Q.
DE
= DEc
+ DEp
+ DU
= W + Q
sous
forme différentielle, cela donne :
dE + dEc + dEp + dU = d
W + dQ
où :
dE représente la différentielle totale exacte de la fonction détat ;
dW
et dQ
représentent des formes différentielles.
La
variation dénergie totale DE
ne dépend que de létat final et de létat initial de la
transformation et non du chemin suivi contrairement aux quantités
W et Q.
2. CONSÉQUENCES
Lénergie
totale dun système isolé se conserve.
dE = O
Pour
un cycle :
DE = W + Q = O
Ce résultat est appelé principe de léquivalence.
Pour
un système fermé, non soumis à des forces extérieures dérivant
dun potentiel, le bilan dénergie prend la forme :
DEc + DU
= W + Q
Pour
un système fermé en labsence de variation dénergie cinétique
macroscopique et non soumis à des forces extérieures dérivant
dun potentiel, le bilan dénergie prend la forme de
lexpression bien connue :
DU
= W + Q
Sous
forme différentielle, cela donne :
dU = dW
+ dQ
La fonction énergie interne est alors une grandeur extensive
conservative.
3. TRAVAIL
3.1. Travail élémentaire des forces extérieures
Le
travail élémentaire des forces extérieures de contact sur un élément
de surface du système lors du déplacement
 de cet élément sécrit :
de cet élément sécrit :
dW
=
 .
.
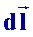
Le
travail des forces de pression représente un cas particulier
important.
3.2. Travail élémentaire des forces extérieures de pression
Le
travail des forces de pression extérieures lors du déplacement élémentaires
 dun élément de paroi de surface dS est :
dun élément de paroi de surface dS est :
dW
= - pext .dV
Où
dV représente la variation de volume du système.
Lors
dune transformation isochore, le système est mécaniquement isolé.
3.3. Travail élémentaire des forces extérieures de pression lors
dune transformation quasi statique.
Lors
dune transformation quasi statique, la pression p du système est
égale à la pression extérieure pext :
dW = - p dV

Le
bilan énergétique sécrit alors, pour un système fermé soumis
aux seules forces de pression,
dU = dQ
- pdV
3.4. Autres expressions du travail élémentaire
Des
systèmes différents décrits par dautres variables peuvent être
considérés (cf. tableau ci-dessous).
|
Système
|
Variable
intensive
|
Variable
extensive
|
Travail
|
|
Fil
tendu
|
Force
de traction F
(N)
|
Longueur
l
(m)
|
dW
= F dl
|
|
Surface
dun liquide
|
Tension
superficielle
A
(N.m 1)
|
Surface
S
(m²)
|
dW
= A dS
|
|
Pile
réversible
|
F.é.m.
E
(V)
|
Charge
Q
(C)
|
dW
= E dq
|
On
remarque lanalogie entre les expressions de ces différents
travaux : le travail élémentaire apparaît toujours comme le
produit dune variable intensive Yi , par la variation
élémentaire dune variable extensive Xi. Ces deux
variables sont dites conjuguées.
Le
travail élémentaire total accompli sur un système sexprime
alors par :
dW
=

Le
travail dépend du chemin suivi. Lunité de travail est le joule
(J).
4. CHALEUR
Les
échanges dénergie non réductibles à un travail sappellent
chaleur.
Ce
transfert dénergie se fait sous la forme dénergie cinétique
moléculaire correspondant à une agitation désordonnée.
La
chaleur dépend du chemin suivi. Lunité de chaleur est le joule
(J).
Les
transferts dénergie sous forme de chaleur se font :
-
par conduction dans les fluides et les solides
-
par convection dans les fluides ;
-
par rayonnement.
Dans
le vide, seul le rayonnement intervient.
Ces
transferts existent entre deux corps à températures différentes
mis en contact mais aussi entre une source de chaleur et un corps
subissant un changement détat à température constante.
Pour
un système soumis aux seules forces de pression dans une
transformation quasi-statique isochore, la chaleur sidentifie
avec la variation dénergie interne :
DU
= Qv
5. LENTHALPIE H
On
définit une fonction détat H à partir de lénergie interne
U, de la pression p et du volume V :
H = U + pV
Sous
forme différentielle :
dH = dU + pdV + Vdp
Lunité
denthalpie est le joule (J).
Pour
un système fermé soumis aux seules forces de pression dans une
transformation élémentaire quasi statique :
dH = dQ
+ Vdp
Pour
un tel système, la chaleur sidentifie avec la variation
denthalpie dans une transformation quasi statique isobare :
DH = Qp
Exercices:
Calculer
le travail effectué par 10 moles de gaz parfait, lorsqu'on les
soumet à une dilatation de 1 atm à 0ºC jusqu'à 0.1 atm à 0ºC
selon chacun des chemins suivants:
a)
on diminue la pression extérieure jusqu'à la pression
finale en maintenant le volume constant, puis on laisse le gaz se
dilater à pression constante jusqu'au volume final;
b)
on diminue la pression extérieure jusqu'à une pression
de 0.5 atm en maintenant le volume constant, puis on laisse le gaz
se dilater à pression constante, ensuite on diminue à nouveau la
pression à volume constant jusqu'à la pression finale et on laisse
enfin le gaz se dilater à pression constante;
c)
à température constante T = 0ºC, en maintenant la
pression extérieure égale à chaque instant à la pression du gaz.
Dans ce cas, le processus est conduit par une succession de
variation infiniment petites par rapport à l'état d'équilibre du
système. Le processus peut donc à tout instant être renversé. Le
processus (c) est réversible.
Réponses:
a) wa=-20438 J; b) wb=-29522 J; c) wc=-52291 J
Calculer
le travail effectué lorsque l'on vaporise une mole d'eau liquide à
100ºC sous pression atmosphérique constante. Les volumes spécifiques
du liquide et de la vapeur à 100ºC sont respectivement 1 et 1720
cm3.g-1.
|